理论上讲,任何自发的氧化还原反应都可以设计成原电池。某同学利用 “Cu+2Ag+ =2 Ag +Cu2+ ” 反应设制一个化学电池,如图所示,已知该电池在外电路中,电流从a极流向b极。请回答下列问题:
(1)b极是电池的 极,材料是 ,该极上出现的现象是 ,写出该电极的反应式 。
(2)a可能为
A、铜 B、银 C、铁 D、石墨
(3)c溶液是
A、CuSO4溶液 B、AgNO3溶液 C、酒精溶液
(4)若该反应过程中有0.2mol电子发生转移,则生成Ag为 克。
乳酸(CH3—CHOH—COOH)是人体生理活动的一种代谢产物,其聚合物(聚乳酸)是一种新型可生物降解的高分子材料,主要用于制造可降解纤维、可降解塑料和医用材料。下图是工业上用化学方法对乳酸进行加工处理的过程,其中A、H、G为链状高分子化合物。
物质H的结构简式为 ,回答下列问题:
,回答下列问题:
(1)写出下列物质的结构简式:C,F。
(2)上述反应①~⑦中,②是反应,⑥是反应。(填反应类型)
(3)写出下列反应的化学方程式:
①。
⑦。
(4)隐形眼镜的制作材料,应具有良好的光学性能、良好的透气性能和亲水性。一般采用G来制作隐形眼镜而不用H,其主要理由是。
某化学兴趣小组要完成中和热的测定。
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、0.5mol· L-1盐酸、0.55mol· L-1NaOH溶液,
尚缺少的实验玻璃用品是、。
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?
(填“能”或“否”),其原因是。
(3)他们记录的实验数据如下:
| 实 验 用 品 |
溶 液 温 度 |
中和热 △H |
|||
| t1 |
t2 |
||||
| ① |
50mL0.55mol.L-1NaOH |
50mL.0.5mol.L-1HCl |
20℃ |
23.3℃ |
|
| ② |
50mL0.55mol.L-1NaOH |
50mL.0.5mol.L-1HCl |
20℃ |
23.5℃ |
已知:Q=Cm(t2 -t1),反应后溶液的比热容C为4.18KJ·℃-1· Kg-1,各物质的密度均为1g·cm-3。计算完成上表。
(4)实验中NaOH的浓度比HCl的大,其原因是
(5)若用KOH代替NaOH,对测定结果(填“有”或“无”)影响;若用醋酸代替HCl做实验,则测定结果(填“偏高”“偏低”或“无影响”)。
甲醇是人们开发和利用的一种新能源。已知:
①2H2(g)+O2(g)===2H2O(l) ΔH1=-571.8 kJ/mol;
②CH3OH(g)+1/2O2(g)===CO2(g)+2H2(g)ΔH2=-192.9 kJ/mol。
(1)甲醇蒸气完全燃烧的热化学反应方程式为__________________________。
(2)反应②中的能量变化如图所示,则ΔH2=________ kJ/mol(用E1、E2表示)。
(3)H2(g)的燃烧热为________。
(4)请你分析H2(g)作为能源比甲醇蒸气作为能源的优点:______(写出两点即可)。
某学生取9g淀粉溶于水,为测定淀粉的水解百分率,其程序如图: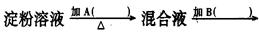

(1)各步所加试剂为:
A、B、C、D。
(2)实验中必须加B溶液的理由是。
(3)当析出2.16g沉淀时,淀粉水解率为。
(1)用食用油炒咸菜的铁锅如果没有洗净,不久会出现红褐色锈斑。则铁锅的锈蚀属于腐蚀(填“析氢”或“吸氧”);该腐蚀正极的电极反应式为;
此反应每转移2mol电子消耗的O2在标准状况下的体积为L。
(2)某同学用碳棒、铜棒和稀硫酸为原材料,实现了在通常条件下不能发生的反应:Cu+H2SO4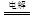 CuSO4+H2↑请在右边方框中画出能够实验这一反应的装置图(作必要的标注);某同学做该实验时,看到碳棒上有气泡产生,铜棒上气泡更多且没有被腐蚀,其原因是。
CuSO4+H2↑请在右边方框中画出能够实验这一反应的装置图(作必要的标注);某同学做该实验时,看到碳棒上有气泡产生,铜棒上气泡更多且没有被腐蚀,其原因是。