下列说法正确的
| A.放热反应在常温下一定容易进行 |
| B.植物的光合作用是把太阳能转化为热能的过程 |
| C.反应是放热还是吸热是由反应物和生成物所具有的能量的相对大小决定的 |
| D.凡是在加热或点燃条件下进行的反应都是吸热反应 |
将a L(标准状况)CO2通入100mL 3mol·L-1 NaOH溶液中,下列各项为通入CO2过程中溶液内发生反应的离子方程式,其中不正确的是
| A.a =3.36时,CO2 + 2OH- = CO32- + H2O |
| B.a =4.48时,2CO2 + 3OH- = CO32- + HCO3- + H2O |
| C.a =6.72时,CO2 + OH- = HCO3- |
| D.a =8.96时,3CO2 + 4OH- = CO32- + 2HCO3- + H2O |
某同学在实验报告中记录下列数据,其中正确的是
| A.用 25mL 量筒量取 18.63mL 盐酸 |
| B.用托盘天平称取 12.15克食盐 |
| C.用标准的 NaOH 溶液滴定未知浓度的盐酸,用去 NaOH 溶液32.30mL |
| D.用 pH 试纸测得某溶液 pH 为 5.0 |
下列化学反应的离子方程式正确的是
| A.AgNO3溶液中加入过量氨水:Ag++2NH3·H2O=Ag(NH3)2++2H2O |
B.少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3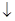 +2HClO +2HClO |
| C.向溴化亚铁溶液中通入少量氯气: 2Br - + Cl2= Br2 + 2 Cl– |
| D.Fe3O4与稀HNO3反应:Fe3O4+8H+==Fe2++2Fe3++4H2O |
X、Y、Z、W四种物质之间有如右图所示的转化关系(部分物质未写全),且已知反应热之间的关系符合等式△H=△H1+△H2。则X、Y可能是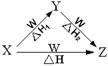
①C、CO ②AlCl3、Al(OH)3
③Fe、Fe(NO3)2 ④Na2CO3、NaHCO3
A.①② B.③④ C.①②③D.①②③④
已知:(1)Al(OH)3电离方程式为:AlO2-+H++H2O Al(OH)3
Al(OH)3 Al3++3OH-
Al3++3OH-
(2)无水AlCl3晶体沸点为182.9℃,溶于水的电离方程式为:AlCl3=Al3++3Cl-
(3)PbSO4难溶于水,易溶于醋酸钠溶液,反应的化学方程式为:
PbSO4+2CH3COONa=Na2SO4+(CH3COO)2Pb
则下列关于Al(OH)3、AlCl3和(CH3COO)2Pb的说法中正确的是
| A.均为强电解质 |
| B.均为弱电解质 |
| C.均为离子化合物 |
| D.均为共价化合物 |