在1100℃,一定容积的密闭容器中发生反应:FeO(s)+CO(g) Fe(s)+CO2(g) △H="a" kJ/mol(a >0),该温度下K=0.263,下列有关该反应的说法正确的是( )
Fe(s)+CO2(g) △H="a" kJ/mol(a >0),该温度下K=0.263,下列有关该反应的说法正确的是( )
| A.若生成1 mol Fe,则吸收的热量小于a kJ |
| B.若升高温度,正反应速率加快,逆反应速率减慢,则化学平衡正向移动 |
| C.若容器内压强不随时间变化,则可以判断该反应已达到化学平衡状态 |
| D.达到化学平衡状态时,若c(CO)="0.100" mol/L,则c(CO2)="0.0263" mol/L |
向含下列微粒的溶液中,①HS-、②Fe2+、③ 、④
、④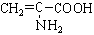 分别加入少量氢氧化钠固体,或少量浓盐酸或几滴酸性KMnO4溶液。(溶液体积变化忽略不计),都使溶液中对应的离子或分子浓度减少的是()
分别加入少量氢氧化钠固体,或少量浓盐酸或几滴酸性KMnO4溶液。(溶液体积变化忽略不计),都使溶液中对应的离子或分子浓度减少的是()
| A.①② | B.②③ | C.①④ | D.③④ |
四氯乙烯对环境有一定的危害,干洗衣服的干洗剂主要成分是四氯乙烯;家用不粘锅内侧涂覆物质的主要成分是聚四氟乙烯。下列关于四氯乙烯和聚四氟乙烯的叙述中正确的是()
| A.它们都属于纯净物 |
| B.它们都能使酸性高锰酸钾溶液褪色 |
| C.它们的分子中都不含氢原子 |
| D.它们都可由乙烯只发生加成反应得到 |
建筑用的钢材在出厂之前都要经过发蓝处理,使其表面生成一层四氧化三铁,其目的是()
| A.增加钢材的硬度 | B.增强钢材的抗腐蚀能力 |
| C.使钢材美观 | D.增加钢材的韧性 |
葡萄糖分子通过缩合反应,将10个葡萄糖分子连接起来所形成的链状化合物的化学式为()
| A.C60H102O51 | B.C60H112O51 | C.C60H120O60 | D.C60H100O52 |
为了进一步提高合成氨的生产效益,科研中最有开发价值的是()。
| A.寻求H2的新来源 | B.研制耐高温高压的新材料合成塔 |
| C.研制低温下活性较大的催化剂 | D.研制高温下活性较大的催化剂 |