工业废气中氮氧化物是造成污染的主要来源之一.为了防治污染,工业上常通入氨气与氮氧化物反应:NOx+NH3→N2+H2O.现有NO、NO2的混合气体3L,可用同温同压下的NH3 3.5L恰好与它完全反应生成N2.则原混合气体中NO和NO2的物质的量之比为
| A.1∶1 | B.1∶2 | C.1∶3 | D.1∶4 |
用NA表示阿伏加德罗常数,下列说法正确的是
| A.在标准状况下,44.8L HF所含有的分子数为2NA |
| B.含2mol H2SO4的浓硫酸与足量铜微热反应,生成SO2分子数为NA |
| C.常温常压下,44g由N2O和CO2组成的混合气体所含的分子数为NA |
| D.1mol羟基和1molOH-含有的电子数都为10NA |
下列离子方程式正确的是
| A.向KAl(SO4)2溶液中滴入Ba(OH)2溶液至SO42-恰好沉淀:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O |
| B.铁红溶于足量HI溶液中:Fe2O3 + 6H+ = 2Fe3+ + 3H2O |
| C.用小苏打治疗胃酸过多:CO32- + 2H+ = CO2↑ + H2O |
| D.铁粉中滴加少量浓硝酸:Fe+3NO3-+6H+=Fe3++3NO2↑+3H2O |
分类是科学研究的重要方法,下列物质分类不正确的是
①混合物:铝热剂、碱石灰、纯净矿泉水、分析纯盐酸
②同素异形体:活性炭、12C、石墨烯、金刚石
③非电解质:乙醇、四氯化碳、氯气、葡萄糖
④原子晶体:金刚石、二氧化硅、碳化硅晶体
⑤胶体:碘酒、淀粉溶液、水雾、纳米材料
A.①③⑤ B.③④⑤ C. ②③⑤ D. ②④⑤
常温下,下列有关叙述正确的是
A.水的离子积KW只与温度有关,但水的电离程度一定会受外加酸、碱、盐的影响
B.若HA的Ka=1.7×10—5,BOH的Kb=1.7×10—5,则HA溶液中的c(H+)与BOH中的c(OH-)相等
C.将0.2mol/L HA溶液和0.1mol/L NaOH溶液等体积混合,则反应后的混合液中:c(OH—)+ c(A—) =c(H+)+ c(HA)
D.Mg(OH)2能溶于NH4Cl浓溶液的主要原因是NH4+结合OH—使沉淀溶解平衡发生移动
某温度下,恒容密闭容器中,发生如下可逆反应:2 E(g)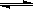 F(g) + x G(g)(正反应放热);若起始时E浓度为a mol/L,F、G浓度均为0,达平衡时E浓度为0.5amol/L,若E的起始浓度改为2amol/L,F、G浓度仍为0,当达到新的平衡时,下列说法正确的是
F(g) + x G(g)(正反应放热);若起始时E浓度为a mol/L,F、G浓度均为0,达平衡时E浓度为0.5amol/L,若E的起始浓度改为2amol/L,F、G浓度仍为0,当达到新的平衡时,下列说法正确的是
| A.升高温度时,正反应速率加快,逆反应速率减慢,平衡逆向移动 |
| B.若x=1,新平衡下E转化率为50% |
| C.若x=2,新平衡下F的平衡浓度为0.5a mol/L |
| D.若x=2,换成恒压容器,则达到平衡所需时间比恒容容器所需时间短 |