现有一瓶久置的标有质量分数为10%的NaOH溶液样品,为探究其变质(NaOH易和空气中的CO2反应生成Na2CO3)的相关问题,利用∪形管设计如下图所示的装置进行实验。
(1)如图46-1所示,若此溶液变质,分别在∪形管的两端滴入HCl溶液和澄清的石灰水时,观察到的现象:a端 ,b端 。
(2)如图46-2所示,取此NaOH样品溶液20g于∪形管中,并在其中加入适量的酚酞试液,通过分液漏斗向∪形管中滴入HCl溶液,当滴入20gHCl溶液时,恰好反应完全。
①滴入稀盐酸过程中,∪形管中的溶液颜色变化为 ;
②恰好完全反应时,生成气体0.22g,试通过计算得出20gNaOH样品溶液中所含Na2CO3的质量。
家庭中长期使用的热水壶底部有一层水垢,主要成 分是碳酸钙和氢氧化镁,可用酸溶液来清除水垢。小明同学想通过实验测定水垢中碳酸钙的含量,他将过量的稀盐酸加入到200 g水垢中(假定水垢中杂质不与酸反应),并将产生的CO2气体全部通入到足量的NaOH溶液中(不考虑盐酸的挥发性),NaOH溶液增加的质量与反应时间的关系如图所示,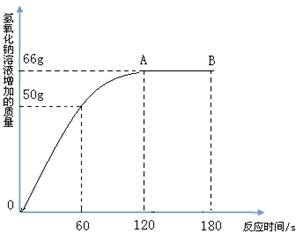
试根据题意回答下列问题:
(1)在滴入稀盐酸的过程中,观察到的一项明显现象是。
(2)从图中可知,NaOH溶液吸收的CO2气体的总质量为_______g。
(3)在水垢中加入稀盐酸时,所发生的中和反应的化学方程式为。
(4)计算水垢中碳酸钙的质量分数(写出相应的计算过程,结果精确到0.1%)。
将29.1g由NaCl和BaCl2组成的固体混合物溶解于94.2ml水中(ρ水 = 1g/cm3),向所得溶液中滴加质量分数为14.2 %的Na2SO4溶液,至恰好完全反应(化学方程式:BaCl2+Na2SO4==BaSO4↓+2NaCl)。右图是所加Na2SO4溶液质量与生成沉淀质量的关系图,计算:
(1)生成沉淀的质量是多少?
(2)所得溶液中溶质的质量分数为多少?
某快递公司违反国家规定快递有毒化学品,因化学品泄露,导致多人伤亡,被称为“夺命快递”,“夺命快递”中的化学品是氟乙酸甲酯(化学式为C3H5FO2),是有毒液体,在燃料、医药、农药等工业领域有着广泛的用途.
(1)氟乙酸甲酯中氟元素的质量分数是。
(2)一般成人接触400mg氟乙酸甲酯就会急性中毒,如果检测到被氟乙酸甲酯污染的某物品上含有氟元素57mg(氟元素都来自氟乙酸甲酯),则接触该污染物品的成年人至少接触到了mg氟乙酸甲酯.
在人类历史发展过程中,金属元素的发现和使用深刻影响了我们的生活、生产等活动。
(1)黄铜(为铜、锌合金)貌似黄金,有人以此冒充黄金行骗,我们称为“假黄金”
①真假黄金可用稀盐酸鉴别,理由是
②也可以“用火灼烧”的办法鉴别其真伪,如果是“假黄金”,观察到的现象是
(2)某研究小组取20 g的“假黄金”进行探究,先将“假黄金”置于烧杯中,然后向烧杯中慢慢加入稀硫酸使其充分反应,直至固体质量不再减少为止,产生的气体和滴加稀硫酸质量的关系曲线如图所示,根据所给信息回答以下问题:
①该“假黄金”中铜的质量是g
②试通过计算求出所用稀硫酸中溶质的质量分数,
(写出计算过程,计算结果精确至0.1 g)
今年我国“世界环境日”的主题是向污染宣战,某化工厂排放的废水中含有碳酸钠,提取50g废水样品于集气瓶中,逐滴加入10%的稀硫酸,至恰好完全反应时,收集到 4.4g二氧化碳,请回答问题:
(1)判断滴加硫酸至恰好反应的依据是。
(2)所消耗的稀硫酸质量是多少?
(3)最后所得溶液中溶质的质量分数是多少?(本小题最后结果取整数)