在一定条件下,向一带活塞的密闭容器中充入2molSO2和1molO2,发生下列反应:
2SO2(g)+O2(g) 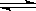 2SO3(g) △H<0,达到平衡状态后,在t1时刻改变条件,化学反应速率随时间变化关系如图。下列对t1时刻改变条件的推断中正确的是
2SO3(g) △H<0,达到平衡状态后,在t1时刻改变条件,化学反应速率随时间变化关系如图。下列对t1时刻改变条件的推断中正确的是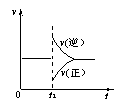
| A.保持压强不变,升高反应温度 |
| B.保持温度不变,增大容器体积 |
| C.保持温度和容器体积不变,充入1molSO3(g) |
| D.保持温度和压强不变,充入1molSO3(g) |
大气污染物氟里昂-12的化学式是CF2Cl2。下面关于氟里昂-12的说法正确的是
| A.它有两种同分异构体 | B.分子中的碳原子是饱和的 |
| C.它属于正四面体的空间结构 | D.是甲烷的一种同系物 |
以下烃中,一氯代物有两种的是
| A.乙烷 | B.异丁烷 | C.新戊烷 | D.苯 |
对于反应A+3B = 2C+D来说,下列反应速率中最快的是
A.v(A)=0.3mol·L-1·min-1 B.v(B)=0.01mol·L-1·s-1
C.v(C)=0.5mol·L-1·min-1 D.v(D)=0.006mol·L-1·s-1
下图为某兴趣小组制作的番茄电池,下列说法正确的是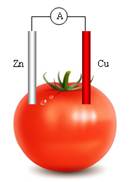
| A.电流由锌通过导线流向铜 |
| B.该装置将电能转化为化学能 |
| C.锌电极发生氧化反应 |
| D.铜电极的质量会不断减少 |
化学与生活、社会密切相关。下列做法正确的是
| A.城市生活垃圾应分类处理,废旧电池回收后集中掩埋,废弃的塑料焚烧处理 |
| B.若将原来燃烧液化石油气的灶具改成烧天然气,应增大空气进气量和减少天然气进入量 |
| C.鉴别棉纺线与羊毛线可用灼烧法鉴别 |
| D.糖尿病人可用氢氧化铜悬浊液检验其新鲜尿样中蔗糖含量的高低 |