下列有关物质性质、结构的表述均正确,且存在因果关系的是
| |
表述Ⅰ |
表述Ⅱ |
| A |
在水中,NaCl的溶解度比I2的溶解度大 |
NaCl晶体中C1—与Na+间的作用力大于碘晶体中分子间的作用力 |
| B |
通常条件下,CH4分子比PbH4分子稳定性高 |
Pb的原子半径比C的大,Pb与H之间的键能比C与H间的小 |
| C |
在形成化合物时,同一主族元素的化合价相同 |
同一主族元素原子的最外层电子数相同 |
| D |
P4O10、C6H12O6溶于水后均不导电 |
P4O10、C6H12O6均属于共价化合物 |
用铂作电极电解1L含有0.4molCuSO4和0.2molNaCl的水溶液,一段时间后在一个电极上得到了19.2 g Cu,在另一极上析出的气体在标况下的体积是
| A.4.48 L | B.5.6 L | C.6.72 L | D.13.44 L |
被称之为“软电池”的纸质电池,采用一个薄层纸片作为传导体,在其一边镀锌,而在其另一边镀二氧化锰。在纸内的离子“流过”水和氧化锌组成的电解液。电池总反应为:
Zn + 2 MnO2 + H2O ="=" ZnO + 2MnO (OH)。下列说法正确的是
| A.该电池的正极为锌 |
| B.该电池反应中二氧化锰起催化剂作用 |
| C.当 0.l mol Zn 完全溶解时,流经电解液的电子个数为 1.204×l023 |
| D.电池正极反应式为: 2MnO2 + 2e -+2H2O ="=2MnO" (OH)+2OH- |
用惰性电极电解下列各稀溶液,经一段时间后,溶液的pH值保持不变的是
| A.AgNO3溶液 | B.NaCl溶液 | C.H2SO4溶液 | D.K2SO4溶液 |
下列变化不能用勒夏特列原理解释的是
| A.向H2S水溶液中加入NaOH有利于S2-增多 |
| B.H2、I2、HI混合气体加压后颜色变深 |
| C.合成氨时将氨液化分离,可提高原料的利用率 |
| D.新制氯水久置后颜色变浅 |
下列溶液一定呈中性的是
A.溶液中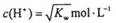 (KW为溶液所处温度时水的离子积常数) (KW为溶液所处温度时水的离子积常数) |
| B.pH=7的溶液 |
| C.使石蕊试液呈紫色的溶液 |
| D.等体积0.1 mol·L-1硫酸与0.1 mol·L-1的氢氧化钠溶液混合后的溶液 |