下列反应的离子方程式正确的是
| A.向KAl(SO4)2溶液中加入Ba(OH)2至SO完全沉淀: 2Ba2++4OH-+Al3++2SO=2BaSO4↓+AlO+2H2O |
| B.偏铝酸钠溶液中加过量HCl:AlO+4H+=Al3++H2O |
| C.向NH4HSO3溶液中滴入适量NaOH溶液:HSO+OH-=SO+ H2O [ |
| D.电镀铜时阳极反应为:Cu2+ + 2e-= Cu |
下列有机物的命名正确的是
| A.2,2—二甲基—1—丁烯 | B.3,3,4-三甲基戊烷 |
| C.2-甲基-3-乙基戊烷 | D.2-氯乙烷 |
下列有关化学用语不能表示2-丁烯的是( )
A.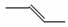 |
B.CH3CH=CHCH3 | C.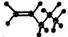 |
D.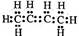 |
居室空气污染的主要来源之一是人们使用的装饰材料、胶合板、内墙涂料释放出的一种刺激性气味的气体,该气体是
| A.CH4 | B.NH3 | C.HCHO | D.SO2 |
常压下乙醇的沸点是78 ℃,乙酸的沸点是118 ℃。下列分离乙醇、乙酸的方案中最佳的一组是( )
| 选项 |
a |
b |
c |
| A |
Na2CO3饱和溶液 |
乙酸钠 |
硫酸 |
| B |
Na2CO3固体 |
乙酸钠 |
盐酸 |
| C |
CaO固体 |
乙酸钙 |
盐酸 |
| D |
CaO固体 |
乙酸钙 |
硫酸 |
下列说法正确的是( )
| A.分离乙醇和乙酸乙酯的混合物,所用玻璃仪器为分液漏斗、烧杯 |
B.用如图所示装置分离CCl4萃取碘水后已分层的有机层和水层 |
| C.用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 |
| D.用如图所示装置除去乙醇中的苯酚 |
