已知25℃、101kPa条件下:①4Al(s)+3O2(g)="2" Al2 O3(s)△H=" —2834.9" kJ·mol-1
②4Al(s)+2O3(g)="2" Al2 O3(s)△H=" —3119.1" kJ·mol-1由此得出的正确结论是()
| A.等质量的O2比O3能量低,由O2变O3为吸热反应 |
| B.等质量的O2比O3能量低,由O2变O3为放热反应 |
| C.O3比O2稳定,由O2变O3为吸热反应 |
| D.O2比O3稳定,由O2变O3为放热反应 |
下列有关电池的说法不正确的是()
| A.手机上用的锂离子电池属于二次电池 |
| B.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极 |
| C.甲醇燃料电池可把化学能转化为电能 |
| D.锌锰干电池中,锌电极是负极 |
下列关于反应速率的说法,错误的是()
| A.反应速率用于衡量化学反应的进行的快慢 |
| B.决定反应速率的主要因素是反应的性质 |
| C.可逆反应达到化学平衡状态时,正、逆反应的速率都为0 |
| D.增大反应物的浓度、提高反应温度都能增大反应速率 |
下列说法错误的是()
| A.燃料的燃烧反应都是放热反应 |
| B.一定量的燃料完全燃烧放出的热量比不完全燃烧放出的热量多 |
| C.放热反应的逆反应一定是吸热反应 |
| D.选择燃料只要考虑燃料热值的大小 |
已知在25℃,101kPa下,1g辛烷C8H18燃烧生成二氧化碳和液态水时放出48.40kJ热量.表示上述反应的热化学方程式正确的是 ( )
A.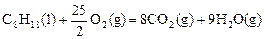 △H=-48.40kJ/mol △H=-48.40kJ/mol |
B.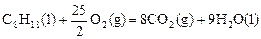 △H=-5518kJ/mol △H=-5518kJ/mol |
C.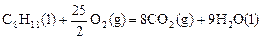 △H=+5518kJ/mol △H=+5518kJ/mol |
D.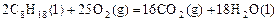 △H=+11036kJ/mol △H=+11036kJ/mol |