通过1个多月的化学学习,应该知道有多种途径可以制取氧气。请根据下列装置,回答问题:
⑴写出标号①②的仪器名称:① ,② 。
⑵实验室要收集较纯净O2,可选用装置是 (填写装置序号);
⑶用排水法收集氧气,当气泡 时,再开始收集;
⑷用高锰酸钾制取O2 的文字表达式为 ,若实验结束发现水槽中的水变成了浅紫红色,你认为产生该现象的原因可能是 ;若实验结束后发现大试管有裂痕,可能的原因是 (写一点)。
若用高锰酸钾制取氧气的操作步骤分为:a给试管加热 b导管移出水面
c检查装置的气密性d排水法收集氧气e熄灭酒精灯 f将反应物加入试管
用带有导管的橡皮塞塞紧并把它固定在铁架台上;其操作的正确顺序是: ___________。
⑸若分解过氧化氢制取氧气,写出反应的文字表达式 可选用的发生装置是 (填写装置序号)。
某兴趣小组利用氨水能使酚酞试液变红的原理,设计如下实验以探究微粒的运动。请回答实验中的有关问题。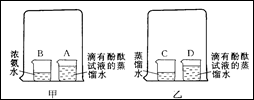
(1)实验I:在盛有少量蒸馏水的小烧杯中滴入2滴~3滴酚酞试液,再向其中滴加浓氨水。由实验I得出的结论有
(2)实验Ⅱ(如上图中甲所示):烧杯A中的现象是;产生这一现象的原因是。
(3)为使实验结论准确可靠,该兴趣小组设计实验Ⅲ(如上图中乙所示)作为对比实验。你认为有无必要,理由是。
同学们已经学习了有关金属的一些知识,对金属的活动性顺序也有 了一定的认识。请运用所学知识参与以下探究并回答相关问题:
【 实验一】将4枚洁净无锈的铁钉分别放入图12中 a、b、c、d 4支试管中。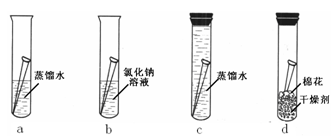
上述实验中,____________试管中的铁钉最易生锈。设计如图d实验的目的是________
________________________________________。铁生锈的主要原因是铁与、
等物质发生了复杂的化学反应。
【 实验二】为了探究Fe、Cu、Al三种金属的活动性顺序,小宁同学做了图13所示的实验.
(1)实验时,为了除去铝和铁表面的氧化物或污物,在插入溶液前应将。
(2)实验时观察到的主要现象是。得出的结论是______________________________。写出其中一种金属与硫酸铜溶液反应的化学方程式。
(3)小成同学认为小宁同学设计的实验不能达到实验目的,原因是
,因此另设计一个实验,才能得出正确的结论。请你设计一个实验并完成下表:
| 操作 |
现象 |
结论 |
| 三种金属活动性由强到弱的顺序是:Al 、Fe、Cu |
某化学兴趣小组按照课本实验方法(如下图),做木炭与氧化铜反应的实验时,发现很难观察到紫红色铜的生成,却往往有暗红色固体出现。他们决定对这个实验进行探究和改进。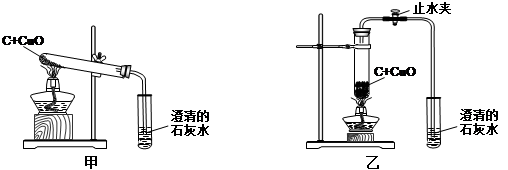
【提出问题】暗红色的固体是什么?如何选择合适条件,使木炭还原氧化铜的实验现象更明显?
【查阅资料】铜有+1和+2两种化合价,通常情况下,氧的化合价为-2,碳的化合价为+4或-4。
【猜想与假设】
(1)同学们认为这种暗红色固体可能是一种化合物,并猜测它的化学式为。
(2)同学们还认为,通过改变反应物的状态、质量比,以及反应装置,可以使该实验现象更加明显,减少出现暗红色固体的情况。
【分析与交流】
(1)小吴建议用超细炭粉与氧化铜粉末进行实验。你认为这样建议的原理是;
反应的化学方程式为:。
(2)小周建议用图乙装置替代甲装置。与甲相比较,乙装置中将试管直立放置的作用是
。
【实验与结论】
同学们决定按改进后的方案进行实验,他们在检验了乙装置的后,往试管中加入已干燥的药品并开始加热,当看到澄清的石灰水刚出现浑浊时,(填“可以”或“不能”)确定氧化铜和炭粉已经开始反应。
不久,即可看到试管底部变红热,停止加热后,仍能看到红热现象,并沿试管底部自下而上蔓延,这个现象说明该反应是(填“吸”或“放”)热反应。
待产物冷却后,同学们终于找到了期待已久的紫红色铜珠,实验获得了圆满成功。
某兴趣小组同学对实验室制取氧气的条件进行如下探究实验.
(1)为探究催化剂的种类对氯酸钾分解速度的影响,甲设计以下对比试验:
I.将3.0gKClO3与1.0gMnO2均匀混合加热
II.将xgKClO3与1.0gCuO均匀混合加热
在相同温度下,比较两组实验产生O2的快慢.
①II中x的值为 .
②若要证明CuO能作为KClO3分解的催化剂,则还要证明在化学反应前后CuO的 和 都不改变.
(2)乙探究了影响双氧水分解速度的某种因素,实验数据记录如表:
| 双氧水的质量 |
双氧水的浓度 |
MnO2的质量 |
相同时间内产生O2的体积 |
| I |
50.0g |
1% |
0.1g |
9mL |
| II |
50.0g |
2% |
0.1g |
16mL |
| III |
50.0g |
4% |
0.1g |
31mL |
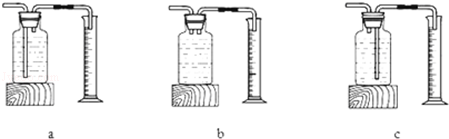
①若用上述装置测生成氧气的体积,则用图 (填“a”“b”或“c”)
②实验结论:在相同条件下, ,双氧水分解得快.
在化学实验室里,酒精是最常用到的一种燃料,其化学式是C2H6O。小明为了证明酒精中含有碳、氢元素,设计并完成如下实验方案。请你帮他完成下面的实验报告。
【实验目的】:证明酒精中含有碳、氢元素。
【实验用品】:酒精灯、火柴、洁净干燥的小烧杯、澄清石灰水
【实验过程及结论】
| 实验步骤 |
实验现象 |
实验结论 |
步骤一:点燃酒精灯,将洁净干燥的小烧杯罩在火焰上方 |
烧杯内壁 有生成; |
证明酒精中含有元素 |
步骤二:迅速取下烧杯,并加入少量,振荡; |
证明酒精中含有碳元素 |