下列离子方程式书写正确的是( )
| A.金属铜与硝酸银溶液反应:Cu+Ag+=Cu2++Ag |
| B.稀硫酸与氢氧化钡溶液反应:Ba2+ +SO42-=BaSO4↓ |
C.氯气与水反应:H2O+Cl2 2H++Cl-+ClO- 2H++Cl-+ClO- |
| D.氯气通入冷的氢氧化钠溶液中:Cl2+2OH- |
将浓度为0.1 溶液加水不断稀释,下列各量始终保持增大的是()
| A. | B. | 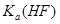 |
C. | 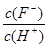 |
D. |  |
700℃时,向容积为2L的密闭容器中充入一定量的
和
,发生反应:
反应过程中测定的部分数据见下表(表中t1>t2):
| 反应时间/min |
||
| 0 |
1.20 |
0.60 |
| t1 |
0.80 |
|
| t2 |
0.20 |
下列说法正确的是()
| A. |
反应在t1min内的平均速率为 |
| B. |
保持其他条件不变,起始时向容器中充入0.60mol 和1.20 mol ,到达平衡时,n(CO2)=0.40 mol。 |
| C. |
保持其他条件不变,向平衡体系中再通入0.20mol ,与原平衡相比,达到新平衡时 转化率增大, 的体积分数减小。 |
| D. |
温度升至800℃,上述反应平衡常数为0.64,则正反应为吸热反应 |
CO与H2在催化剂作用下合成甲醇的反应为:CO(g)+2H2(g)  CH3OH(g)。在容积均为1L的a、b、c、d、e五个密闭容器中分别充入等量的1mol CO和2mol H2混合气体,控温。实验测得相关数据如下图1和图2。
CH3OH(g)。在容积均为1L的a、b、c、d、e五个密闭容器中分别充入等量的1mol CO和2mol H2混合气体,控温。实验测得相关数据如下图1和图2。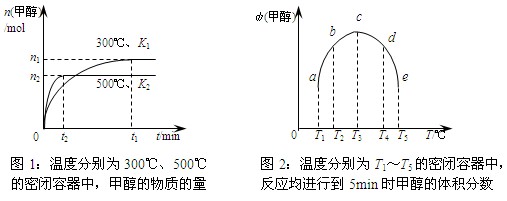
下列有关说法正确的是
| A.该反应的正反应是气体体积减小的吸热反应 |
| B.K1<K2(K为该条件下反应的平衡常数) |
| C.反应进行到5min时,a、b两容器中平衡正向移动,d、e两容器中平衡逆向移动 |
| D.将容器c中的平衡状态转变到容器d中的平衡状态,可采取的措施有升温或减压 |
恒温恒容条件下,下列叙述正确的是
A.相同的甲、乙两容器中分别加入1 g SO2、1 g O2与2 g SO2、2 g O2,发生反应2SO2(g)+O2(g)  SO3(g)达到平衡,SO2的转化率前者大 SO3(g)达到平衡,SO2的转化率前者大 |
B.反应2HI(g)  H2(g)+I2(g)达到平衡,增大HI的物质的量,平衡不移动 H2(g)+I2(g)达到平衡,增大HI的物质的量,平衡不移动 |
C.反应2NO2(g )  N2O4(g)达到平衡时,再向容器内通入一定量的NO2(g),重新达到平衡时,与第一次平衡时相比,NO2的体积分数增大 N2O4(g)达到平衡时,再向容器内通入一定量的NO2(g),重新达到平衡时,与第一次平衡时相比,NO2的体积分数增大 |
D.反应2HI(g)  H2(g)+I2(g)达到平衡,增大HI的物质的量,HI的分解率和体积分数均不变 H2(g)+I2(g)达到平衡,增大HI的物质的量,HI的分解率和体积分数均不变 |
相同温度下,体积均为0.25 L的两个恒容密闭容器中发生可逆反应:N2(g)+3H2(g) 2NH3(g) ΔH=-92.6 kJ·mol-1。实验测得起始、平衡时的有关数据如下表所示:
2NH3(g) ΔH=-92.6 kJ·mol-1。实验测得起始、平衡时的有关数据如下表所示:
| 容器 编号 |
起始时各物质的物质的量/mol |
达平衡时体系能量的变化 |
||
| N2 |
H2 |
NH3 |
||
| ① |
1 |
3 |
0 |
放出热量:23.15 kJ |
| ② |
0.9 |
2.7 |
0.2 |
放出热量:Q |
下列叙述错误的是
A.容器①、②中反应的平衡常数相等
B.平衡时,两个容器中NH3的体积分数均为1/7
C.容器②中达平衡时放出的热量Q=23.15 kJ
D.若容器①的体积为0.5 L,则平衡时放出的热量小于23.15 kJ