含11.2g KOH的稀溶液与1L 0.1mol/L的H2SO4溶液反应放出11.4kJ的热量,下列能正确表示中和热的热化学方程式是
| A.KOH(aq) + 1/2 H2SO4(aq) =1/2K2SO4(aq) + H2O (l);ΔH=-11.46kJ/mol |
| B.2KOH(s) +H2SO4(aq) = K2SO4(aq) + 2H2O (l);ΔH=-114.6kJ/mol |
| C.2KOH(aq) +H2SO4 =K2SO4(aq) + H2O (l) ;ΔH=+114.6kJ/mol |
| D.KOH (aq) + 1/2 H2SO4(aq) =" 1/2" K2SO4(aq) + H2O (l) ;ΔH=-57.3kJ/mol |
有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期,Z、M同主族;X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的内层电子总数是最外层电子数的5倍。下列说法中不正确的是
| A.W、M的某种单质可作为水处理中的消毒剂 |
| B.电解YW2的熔融物可制得Y和W的单质 |
| C.相同条件下,W的氢化物水溶液酸性比Z弱 |
| D.X、M两种元素形成的一种化合物与水反应可生成M的某种单质 |
下列叙述正确的是
| A.0.1mol·L-1CH3COONa溶液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| B.NH4Cl溶液加水稀释后,恢复至原温度,pH和KW均增大 |
| C.pH=4的CH3COOH溶液和pH=4的NH4Cl溶液中,c(H+)不相等 |
| D.在NaHCO3溶液中:c(OH-)+c(CO32-)=c(H+)+c(H2CO3) |
设NA为阿伏伽德罗常数的数值,下列说法正确的是
| A.常温下,23g NO2含有NA个氧原子 |
| B.标准状况下,11.2L SO3中含有的分子数为0.5NA |
| C.1 mol Cl2做氧化剂转移的电子数是NA |
| D.1L 0.1mol/L-1的氨水中含OH―离子数为0.1NA个 |
下列化学用语正确的是
A.乙烯分子的电子式 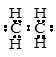 |
B.硫原子的结构示意图  |
| C.淀粉的化学式 (C6H10O5)n |
| D.硫酸铁的电离方程式 Fe2(SO4)3 = 2Fe2+ + 3SO42ˉ |
有6.85g铅的氧化物,用足量的CO 在高温下将其还原,把生成的全部CO2通入到足量的澄清的石灰水中得到4.00g固体沉淀物,这种铅的氧化物的化学式为
| A.PbO | B.PbO2 |
| C.Pb3O4 | D. Pb3O4和PbO2的混合物 |