高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O  3Zn(OH)2 + 2Fe(OH)3 + 4KOH
3Zn(OH)2 + 2Fe(OH)3 + 4KOH
下列叙述不正确的是( )
| A.放电时负极反应为:Zn-2e—+2OH—=Zn(OH)2 |
| B.充电时阳极反应为:Fe(OH)3 -3e—+ 5OH—=FeO42-+ 4H2O |
| C.放电时每转移3mol电子,正极有1molK2FeO4被氧化 |
| D.放电时正极附近溶液的碱性增强 |
100mL0.03mol/LNa2SO4溶液和50 mL0.02 mol/LAl2(SO4)3溶液混合(不考虑水的电离),下列说法中正确的是(不考虑混合后溶液体积的变化):
| A.混合液中c(SO42-)为0.04 mol∙L-1 |
| B.原Al2(SO4)3溶液中c(Al 3+)与100 mL 0.02 mol∙L-1Al (NO3)3中c(Al 3+)相等 |
| C.混合后的溶液中含有0.003 molNa+ |
D.混 合后溶液中c(Na+)为0.02mol/L 合后溶液中c(Na+)为0.02mol/L |
V L硫酸铝溶液中含Al3+的质量为m g,则溶液中SO42-的物质的量浓度为:
A.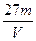 mol·L-1 mol·L-1 |
B. mol·L-1 mol·L-1 |
C.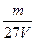 mol·L-1 mol·L-1 |
D.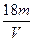 mol·L-1 mol·L-1 |
氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂等。下列反应与Br2+SO2+2H2O=H2SO4+2HBr相比较,水的作用相同的是
能正确表示下列反应的离子方程式是
| A.利用腐蚀法制作印刷线路板:Fe3++Cu = Fe2++Cu2+ |
| B.石灰乳与Na2CO3溶液混合:Ca2++CO32- = CaCO3↓ |
| C.碳酸钙溶于醋酸:CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2↑+H2O |
D.NaHCO3溶液中加入过量的Ba(OH)2溶液:2 +Ba2++2OH-=BaCO3↓+2H2O+ +Ba2++2OH-=BaCO3↓+2H2O+ |
NA为阿伏伽德罗常数,下列叙述错误的是
A.18gH2O中含的质子数为10NA
B.标准状况下,22.4L空气含有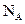
 个单质分子
个单质分子
C .46gNO2和N2O4混合气体中含有原子总数为3NA
.46gNO2和N2O4混合气体中含有原子总数为3NA
D.由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA