Mn、Fe均为第四周期过渡元素,两元素的部分电离能(I)数据列于下表:
| 元素 |
25Mn |
26Fe |
|
| 电离能/kJ·mol-1 |
I1 |
717 |
759 |
| I2 |
1509 |
1561 |
|
| I3 |
3248 |
2957 |
回答下列问题:
(1)Mn元素外围电子层的电子排布式为 ,比较两元素的I2、I3可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难。对此,你的解释是 。
(2)Fe原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物,则与Fe原子或离子形成配合物的分子或离子应具备的条件是 。
(3)三氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华。易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断三氯化铁晶体为 晶体。
(4)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如右图所示。体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为 。
大气污染问题日益引起全民关注。
(1)PM2.5是指大气中直径小于或等于2.5μm(1μm ="103" nm)的颗粒物。下列说法 不正确的是_________ (填字母序号)。
a.PM2.5主要来源于火力发电、工业生产、汽车尾气排放等过程
b.PM2.5颗粒小,所以对人体无害
c.直径介于1 ~ 2.5μm的颗粒物分散到空气中可形成胶体
d.推广使用电动汽车,可以减少PM2.5的污染
(2)北京科研工作者用五年时间研究出利用石灰乳除工业燃煤尾气中的硫(SO2、SO3)和氮(NO、NO2)的新工艺,既能净化尾气,又能获得应用广泛的CaSO4和Ca(NO2)2。
① 硫酸型酸雨的形成过程是大气中的SO2溶于雨水生成某种弱酸,在空气中经催化氧化生成硫酸,该过程中反应的化学方程式为________________________ 、_______________ 。
② CaSO4可以调节水泥的硬化时间。尾气中2molSO2被石灰乳逐渐吸收最终生成了1mol CaSO4,该过程中转移的电子数目为_________________________
③ Ca(NO2)2可制成混凝土防冻剂、钢筋阻锈剂等。尾气中NO、NO2与石灰乳反应生成Ca(NO2)2的化学方程式______________________________ 。
(3)人类活动产生的CO2长期积累,威胁到生态环境,其减排问题受到全世界关注。
工业上常用高浓度的K2CO3溶液吸收CO2,得溶液X, 再利用电解法使K2CO3溶液再生,其装置示意图如下:
①在阳极区发生的反应包括____________和 H ++ HCO3-= H2O + CO2↑。
②简述CO32-在阴极区再生的原理____________________________ 。
③再生装置中产生的CO2和H2在一定条件下反应生成甲醇,工业上利用该反应合成甲醇。 已知:25 ℃,101 KPa下: H2(g) + 1/2 O2(g) =H2O(g) Δ H1=" -242" kJ/mol
CH3OH(g) + 3/2 O2(g) =CO2 (g) + 2 H2O(g) Δ H2=" -676" kJ/mol
写出CO2和H2生成气态甲醇等产物的热化学方程式________________________ 。
铁的发现和大规模使用,是人类发展史上的一个光辉里程碑,它把人类从石器时代、青铜器时代带到了铁器时代,推动了人类文明的发展。
(1)高铁酸钠(Na2FeO4)是水处理过程中的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原成三价铁离子达到净水的目的。按要求回答下列问题: 高铁酸钠主要通过如下反应制取:
2Fe(OH)3 + 3NaClO + 4NaOH = 2Na2FeO4 + 3X + 5H2O,
则X 的化学式________________ ,反应中被氧化的物质是_____________ (写化学式)。
(2)铁红颜料跟某些油料混合,可以制成防锈油漆。以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO 等,用硫酸渣制备铁红(Fe2O3)的过程如下:
①酸溶过程中Fe2O3与稀硫酸反应的化学方程式为_______________________ ;
“滤渣A”主要成份的化学式为____________________ 。
②还原过程中加入FeS2的目的是将溶液中的Fe3+还原为Fe2+,而本身被氧化为H2SO4,请完成该反应的离子方程式:
___ FeS2 + ___Fe3 + +___ H2O = ___Fe2 + +___ SO42- + ___。
③氧化过程中,O2、NaOH与Fe2+反应的离子方程式为________________ 。
④为了确保铁红的质量和纯度,氧化过程需要调节溶液的pH的范围是3.2~3.8, 
如果pH过大,可能引起的后果是____________(几种离子沉淀的pH见上表);滤液B可以回收的物质有___________(写化学式) 。
下列各表述与示意图不一致的是
(1)图①表示向含Mg2+、Al3+、NH4+的盐溶液中滴加NaOH溶液时,沉淀的物质的量和NaOH的体积的关系图。则三种离子的物质的量之比为______________________;
图②中曲线表示某反应过程的能量变化,当物质A(g)与B(g)反应生成物质C时,△H____0,若使用正催化剂,E值会_____________(增大、减小、不变)。
(2)在Cu2O/ZnO做催化剂的条件下,将CO(g)和H2O(g)充入容积为2L的密闭容器中合成CH3OH(g) ,反应过程中,CH3OH的物质的量(n)与时间(t)及温度的关系如图.根据题意回答下列问题:
①反应达到平衡时,平衡常数表达式K=______________;升高温度,K值____________(填“增大”、“减小”或“不变”).
②在500℃,从反应开始到平衡,氢气的平均反应速率v(H2)= ____________;
③若其它条件不变,对处于Z点的体系,将体积压缩至原来的 1/2,达到新的平衡后,下列有关该体系的说法正确的是_________;
a.氢气的浓度与原平衡比减少 b.正、逆反应速率都加快
c.甲醇的物质的量增加d.重新平衡时n(H2) /n(CH3OH)增大
④据研究,反应过程中起催化作用的为Cu2O,反应体系中含少量的CO2有利于维持Cu2O的量不变,原因是_________________;(写出相关的化学方程式并辅以必要的文字说明).
Ⅰ在右图所示装置中,U形管内装满稀H2SO4,a为铁电极,b为多孔石墨电极。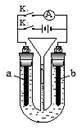
①断开K2接通K1时,为_____________极,b电极上的电极反应式为________________;
②断开K1时接通K2,a为_____________极;该电极上的电极反应式是____________一段时间后,溶液的pH_________(填“增大”、“减小”或“不变”)
Ⅱ、双隔膜电解池的结构示意简图如图所示,利用该装置可以电解硫酸钠溶液以制取硫酸和氢氧化钠,并得到氢气和氧气。
a气体为______________,B溶液为________________;C隔膜为____________(阳离子交换膜、阴离子交换膜),该电解反应的总方程式可表示为_______________________。
某有机物ag与0.8mol O2在密闭容器中充分混合后点燃。待充分反应后,将产物中的H2O(g)和其它气态产物先缓慢通过足量澄清石灰水,产生40g白色沉淀,溶液质量减少0.8g。余下气体通过浓硫酸干燥后,再缓慢通过足量灼热CuO,固体由黑变红。将产生的气体又缓慢通过足量过氧化钠,充分反应后固体质量增加11.2g且只有氧气放出(假设每一步都充分反应或吸收)。请回答下列问题:
①通过计算确定该有机物化学式为 。
②若ag该有机物恰好与18.4g金属钠完全反应,试确定该有机物的结构简式 。
③若0.4mol该有机物恰好与9.2g金属钠完全反应,试确定该有机物的结构简式 。
(已知① 醚不与钠反应 ②一个碳原子上同时连2个或多个羟基是不稳定的)