已知Ba【Al(OH)4】2可溶于水。右图表示的是向A12(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加入Ba(OH)2的物质的量x的关系。下列有关叙述正确的是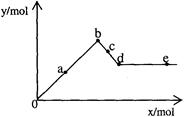
A a-b时沉淀的物质的量:A1(OH)3比BaSO4多
B d-e时溶液中离子的物质的量:Ba2+可能等于OH-
C a-d时沉淀的物质的量:BaSO4可能小于A1(OH)3
D c-d时溶液中离子的物质的量:【Al(OH)4】-比Ba2+少
膦(PH3)又称磷化氢,在常温下是一种无色有大蒜臭味的有毒气体,电石气的杂质中常含有磷化氢。以下关于PH3的叙述正确的是
| A.PH3分子的P-H键是非极性键 |
| B.PH3比NH3稳定 |
| C.PH3的分子构型是正四面体形 |
| D.PH3分子中有未成键的孤对电子 |
X、Y、Z是3种短周期元素,其中X、Y位于同一族,Y、Z处于同一周期。X原子的外围电子排布式为nSnnPn+2。Z原子的核电荷数是最外层电子数的三倍。下列说法正确的是
| A.原子序数由大到小的顺序为Z<Y<X |
| B.Y元素最高价氧化物对应水化物的化学式可表示为H3YO4 |
| C.3种元素的气态氢化物中Z的气态氢化物最稳定 |
| D.原子半径由大到小的顺序为Z>Y>X |
下列叙述正确的是
| A.同一主族的元素,原子半径越大,其单质的熔点一定越高 |
| B.同一周期元素的原子,半径越小越容易失去电子 |
| C.同一主族的元素的氢化物,相对分子质量越大,它的沸点一定越高 |
| D.稀有气体元素的原子序数越大,其单质的沸点一定越高 |
已知硫酸亚铁溶液中加入过氧化钠时发生反应:4Fe2++4Na2O2+6H2O===4Fe(OH)3↓+O2↑+8Na+,则下列说法正确的是
| A.该反应中Fe2+是还原剂,O2是还原产物 |
| B.4 mol Na2O2在反应中共得到8NA个电子 |
| C.Fe(OH)3是氧化产物,每生成1 mol O2反应过程中共转移6 mol电子 |
| D.反应过程中可以看到白色沉淀转化为灰绿色再转化为红褐色沉淀 |