有关热化学方程式书写与对应表述均正确的是
| A.稀醋酸与0.1 mol/LNaOH溶液反应:H+(aq)+OH-(aq) = H2O(l)△H = -57.3kJ/mol |
| B.氢气的燃烧热为285.5 kJ/mol,则水分解的热化学方程式: 2H2O(l)=2H2(g)+O2(g)△H = +285.5kJ/mol |
| C.密闭容器中,9.6 g硫粉与11. 2 g铁粉混合加热生成硫化亚铁17 .6 g时,放出19.12 kJ热量。则Fe(s)+S(s)=FeS(s)△H=" -" 95.6KJ/mol |
| D.已知2C(s)+O2(g)=2CO(g)△H=-221 kJ/mol,则可知C的燃烧热为110.5 kJ/mol |
Cu2S与一定浓度的HNO3反应,生成Cu(NO3)2、CuSO4、NO2、NO和H2O,当NO2和NO的物质的量之比为1∶1时,实际参加反应的Cu2S与HNO3的物质的量之比为
| A.1∶7 | B.1∶9 | C.1∶5 | D.2∶9 |
工业上从含硒的废料中提取硒的方法之一是用硫酸和硝酸钠处理废料,获得亚硝酸和少量硒酸,再与盐酸共热,硒酸被转化为亚硒酸:2HCl+H2SeO4 H2SeO3+Cl2↑+H2O,通SO2于亚硒酸溶液中,单质硒即析出。据此,下列叙述正确的是
H2SeO3+Cl2↑+H2O,通SO2于亚硒酸溶液中,单质硒即析出。据此,下列叙述正确的是
| A.H2SeO4氧化性强于Cl2 | B.亚硒酸氧化性强于H2SO3 |
| C.二氧化硒的还原性强于二氧化硫 | D.析出1 mol Se需H2SeO3,SO2,H2O各1 mol |
在研究金属钠与水的反应实验中,反应过程观察到的实 验现象与金属钠的下列性质无关的是
验现象与金属钠的下列性质无关的是
A.熔点低 |
B.密度小 | C.硬度小 | D.化学性质活泼 |
下列反应不属于四种基本反应类型,但属于氧化还原反应的是
A.3CO+Fe2O3  2Fe+3CO2 2Fe+3CO2 |
B.AgNO3+NaCl="AgCl↓" +NaNO3 |
| C.Cl2+2NaBr=2NaCl+Br2 | D.2Cu + O2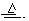 2CuO 2CuO |
有a克Na2CO3 和NaHCO3混合物,下列实验方案中可测定其中Na2CO3质量分数的是
和NaHCO3混合物,下列实验方案中可测定其中Na2CO3质量分数的是
①将混合物与足量稀盐酸充分反应,逸出气体用碱石灰吸收,碱石灰增重b克
②将混合物充分加热,固体质量减少b克
③将混合物与足量BaCl2溶液充分反应,过滤、洗涤、烘干,得b克固体。
④将混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,碱石灰增重b克
| A.①② | B.②③ | C.②④ | D.③④ |