把下列四种碳酸氢钠溶液分别加入四个盛有10 mL 2 mol·L-1盐酸的烧杯中,均加水稀释到50 mL,此时碳酸氢钠和盐酸反应,其中反应开始时速率最大的是( )
| A.10 ℃ 20 mL 3 mol·L-1的碳酸氢钠溶液 | B.20 ℃ 30 mL 2 mol·L-1的碳酸氢钠溶液 |
| C.20 ℃ 10 mL 4 mol·L-1的碳酸氢钠溶液 | D.10 ℃ 20 mL 2 mol·L-1的碳酸氢钠溶液 |
已知R、M、T、G、J为原子序数依次增大且相邻的同一短周期主族元素。下列说法一定正确的是()
| A.若R、M的最高价氧化物的水化物是碱,则M(OH)n+1的碱性比R(OH)n的碱性强 |
| B.若T(OH)n为两性氢氧化物,则元素G形成的单质是半导体 |
C.若J的氢化物是常见的强电解质,则M单 质是光导纤维的主要成分 质是光导纤维的主要成分 |
| D.若M的最高正价为+4,则五种元素全是非金属元素 |
.金属材料在日常生活以及生产中有着广泛的运用。下列关于金属的一些说法不正确的是( )
| A.合金的性质与其成分金属的性质不完全相同 |
| B.工业上金属Mg、Al都是用电解熔融的氯化物制得的 |
| C.金属冶炼的本质是金属阳离子得到电子变成金属原子 |
| D.越活泼的金属越难冶炼 |
T℃时,某一气态平衡体系中含有X(g)、Y(g)、Z(g)、W(g)四种物质,此温度下发生反应的平衡常数表达式为: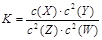 ,有关该平衡体系的说法正确的是()
,有关该平衡体系的说法正确的是()
| A.升高温度,平衡常数K增大 |
B.升高温度,若混合气体的平 均相对分子质量变小,则正反应是放热反应 均相对分子质量变小,则正反应是放热反应 |
| C.增大压强,W(g)体积分数增加 |
| D.增大X(g)浓度,平衡向正反应方向移动 |
.下列实验能达到预期目的的是()
| 编号 |
实验内容 |
实验目的 |
| A |
将SO2通入溴水,溴水褪色后加热观察能否恢复原色 |
验证SO2漂白的可逆性 |
| B |
将氯水加入淀粉KI溶液中 |
验证Cl的非金属性比I强 |
| C |
把铁块和铜块用导线连接插入浓硝酸中 |
组成原电池验证Fe比Cu活泼 |
| D |
加热氯化铵和碘单质的固体混合物 |
分离除去碘单质 |
一定条件下,体积为2L的密闭容器中,1mol A和1mo1 B进行反应:
A(g)+3B(g)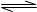 2C(g)经2分钟反应达到平衡,此时生成0.2mol C。
2C(g)经2分钟反应达到平衡,此时生成0.2mol C。
下列说法正确的是()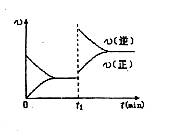
A.反应开始至2分钟时,以B浓度变化表示的反应速率为0.05mol/(L.min)
B.反应开始至2分钟时,A的转化率为5%
C.若其他条件不变,升高温度,A的体积分数增大,则该反应的△H<0
D.若其他条件不变,增大压强,化学反应速率的变化符合右侧示意图