根据图示填空
(1)化合物A含有的官能团 。
(2)1 mol A与2 mol H2反应生成1 mol E,其反应方程式是 。
(3)与A具有相同官能团的A的同分异构体的结构简式是 。
(4) B在酸性条件下与Br2反应得到D.D的结构简式是 。
(5)F的结构简式是 。由E生成F的反应类型是 。
可用于分离或提纯物质的方法有:①过滤,②蒸馏,③加热,④分液(在下列横线上填写分离提纯的合理方法的序号)。
(1)除去石灰水中悬浮的CaCO3颗粒:________。
(2)除去NaCl晶体中混有的碘单质:________。
(3)分离汽油和煤油的混合物:________。
(4)分离水和苯的混合物:________。
【化学一有机化学基础】(15分)尼龙是目前世界上产量最大、应用范围最广、性能比较优异的一种合成纤维。以X为原料合成尼龙-66的流程如下: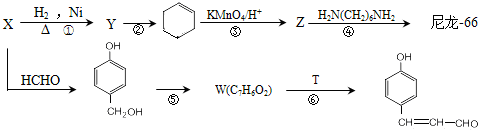
已知部分信息如下:
I.Z的化学式为C6H10O4。
Ⅱ.X和浓溴水反应产生白色沉淀。
Ⅲ.某些醛与醛之间能发生羟醛缩合反应,例如:
RCHO+CH3CHO RCH(OH)CH2CHO
RCH(OH)CH2CHO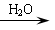 RCH=CHCHO+H2O
RCH=CHCHO+H2O
请回答下列问题:
(1)X的化学名称为_______。W的结构简式为_______。T的分子式为_________。
(2)反应②的条件为__________。
(3)写出反应④的化学方程式___________。反应⑤的类型为___________。
(4)G是Z少一个碳原子的同系物,M是G的同分异构体。M既能发生银镜反应和水解反应。又能和碳酸氢钠反应产生气体,M的结构共有种,其中,在核磁共振氢谱上有3个峰的结构简式为___。
【化学一物质结构与性质】(15分)周期表中前四周期元素R、W、X、Y、Z的原子序数依次递增。R的基志原子中占据哑铃形原子轨道的电子数为1;W的氢化物的沸点比同族其它元素氢化物的沸点高;X2+与W2-具有相同的电子层结构;Y元素原子的3P能级处于半充满状态;Z+的电子层都充满电子。请回答下列问题: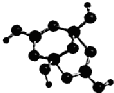
(1)写出Z的基态原子外围电子排布__________。
(2)R的某种钠盐晶体,其阴离子Am-(含R、W、氢三种元素)的球棍模型如上图所示:在Am-中,R原子轨道杂化类型有_______;m=_____。(填数字)
(3)经X射线探明,X与W形成化合物的晶体结构与NaCl的晶体结构相似,X2+的配位原子所构成的立体几何构型为____________。
(4)往Z的硫酸盐溶液中加入过量氨水,可生成[Z(NH3)4]SO4,下列说法正确的是_______。
| A.[Z(NH3)4]SO4中所含的化学键有离子键、极性键和配位键 |
| B.在[Z(NH3)4]2+中Z2+给出孤对电子,NH3提供空轨道 |
| C.[Z(NH3)4]SO4组成元素中第一电离能最大的是氧元素 |
| D.SO42-与PO43-互为等电子体,空间构型均为四面体 |
(5)固体YCl5的结构实际上是YCl4+和YCl6-构成的离子晶体,其晶体结构与CsCl相似.若晶胞边长为apm,则晶胞的密度为____g•cm-3。(已知阿伏伽德罗常数为NA,用含a和NA的代数式表示)
【化学—化学与技术】甲酸钠广泛用作催化剂、稳定合成剂、印染行业的还原剂,还可用于生产保险粉、草酸和甲酸。甲酸钠用电石炉废气(75%~90%CO,以及少量CO2、H2S、N2、CH4等)合成,其合成部分工艺流程如下: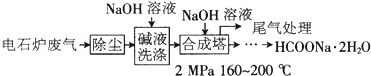
(1)上述工艺用碱液洗涤的目的是___________,可能发生的反应有_______(写两个化学方程式)。
(2)上述合成工艺中采用循环喷射吸收合成,其目的是_________;最后尾气主要成分是______。
(3)甲酸钠高温时分解制取草酸钠(Na2C2O4)的化学方程式为________。
(4)在甲酸钠、氢氧化钠混合溶液中通入二氧化硫气体,可得到重要的工业产品保险粉(Na2S2O4),同时产生二氧化碳气体,该反应的离子方程式为____________。
(5)某厂测知合成塔中甲酸钠生产产率为40%,要制得溶质质量分数为5%的HCOONa溶液1吨,需要CO在标况下的体积为___________。
火力发电厂释放出大量氮氧化合物(NOx)、SO2和CO2等气体会造成环境问题。对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的。
(1)脱硝。利用甲烷催化还原NOx:
CH4(g)+ 4NO2(g)=4NO(g)+ CO2(g)+ 2H2O(g) △H1=-574 kJ/mol
CH4(g)+ 4NO(g)=2N2(g)+ CO2(g)+ 2H2O(g)△H2=-1160 kJ/mol
甲烷直接将NO2还原为N2的热化学方程式为 。
(2)脱碳。将CO2转化为甲醇:CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H3
CH3OH(g)+H2O(g)△H3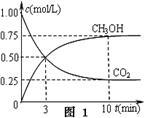
①在一恒温恒容密闭容器中充入1 mol CO2和3 mol H2进行上述反应。测得CO2和CH3OH(g)浓度随时间变化如图1所示。回答:0~10 min内,氢气的平均反应速率为 mol/(L·min);第10 min后,保持温度不变,向该密闭容器中再充入1 mol CO2(g)和1 mol H2O(g),则平衡 (填“正向”、“逆向”或“不”)移动。
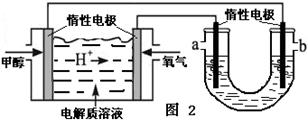
②如图2,25℃时以甲醇燃料电池(电解质溶液为稀硫酸)为电源来电解300mL 某NaCl溶液,正极反应式为 。在电解一段时间后,NaCl溶液的pH值变为13(假设NaCl溶液的体积不变),则理论上消耗甲醇的物质的量为 mol。
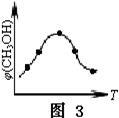
③取五份等体积的CO2和H2的混合气体(物质的量之比均为1∶3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如图3所示,则上述CO2转化为甲醇的反应的△H3 0(填“>”、“<”或“=”)。
(3)脱硫。燃煤废气经脱硝、脱碳后,与一定量氨气、空气反应,生成硫酸铵。硫酸铵水溶液呈酸性的原因是 (用离子方程式表示);室温时,向(NH4)2SO4,溶液中滴人NaOH溶液至溶液呈中性,则所得溶液中微粒浓度大小关系c(Na+) c(NH3·H2O)。(填“>”、“<”或“=”)