下列说法中①物质发生化学反应都伴随着能量变化;②伴有能量变化的物质变化都是化学变化;③酸和碱发生中和反应生成1mol水时所释放的热量称为中和热;④H20比H2S
的沸点高是因为H20中含有的化学键比 H2S强;⑤Al与稀盐酸反应是放热反应;⑥
Ba(OH)2.8H2O晶体与NH4Cl固体的反应是放热反应;⑦CaCO3受热分解是吸热反应; ⑧
CaO与水的反应是放热反应;⑨放热反应在常温下一定很容易发生,其中正确的组合( )
| A.①②⑤⑥⑦⑩ | B.①③⑤⑦⑧ |
| C.①④⑤⑦⑧⑨ | D.①③⑤⑥⑦⑧⑨ |
常温下,下列各组离子一定能大量共存的是
| A.滴加甲基橙试剂显红色的溶液中:Na+、Fe2+、Cl-、NO3- |
| B.c(H+)=10-12 mol·L-1的溶液:NH4+、Al3+、NO3-、SO42- |
| C.c(OH-)/ c(H+)=1012的溶液中:K+、Ba2+、Cl-、Br- |
| D.由水电离的c(H+)=1.0×10-13 mol·L-1的溶液中:Ca2+、K+、Cl-、HCO3- |
向含有下列离子的溶液中分别加少量的Na2O固体后,该离子数目能增加的是
| A.HS- | B.CO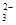 |
C.NH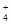 |
D.NO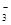 |
某种外围电子排布式为2s22p5的元素,下列有关它的描述正确的有
| A.原子序数为7 | B.在周期表中第一电离能最小 |
| C.在周期表中原子半径最小 | D.在周期表中电负性最大 |
下列溶液一定呈中性的是
| A.pH=7的溶液 | B.由强酸、强碱等物质的量反应制得的溶液 |
| C.c(H+) = c(OH-)的溶液 | D.非电解质溶于水得到的溶液 |
下列物质中,属于强电解质的是
| A.BaSO4 | B.Cu | C.SO3 | D.H2SO3 |