下图是氨气与氯化氢反应的装置。抽走玻璃片充分反应,反应中有关物理量的描述正确的是(NA表示阿伏加德罗常数)
| A.气体反应物的总体积为0.224 L | B.生成物的分子个数为0.005 NA |
| C.产物中的N-H键个数为0.02NA | D.加水溶解后所得溶液中NH4+数目为0.005 NA |
NA表示阿伏加德罗常数的值,下列说法中正确的是
| A.1 mol Zn与足量任意浓度的硫酸反应转移电子数均是2 NA |
| B.在常温常压下1 mol C7H16中含有共价键的总数目是23 NA |
| C.0.1 mol FeCl3完全水解生成Fe(OH)3胶体粒子数目为0.1NA |
| D.33.6 L 盐酸在标准状况下所含有HCl分子的数目为1.5 NA |
下面说法中正确的是
A.标有“ ”的包装材料可以用来包装食品 ”的包装材料可以用来包装食品 |
| B.酒精消毒原理是将病毒彻底氧化 |
| C.GaN中的氮和镓均属于第IIIA族元素 |
| D.麦芽糖的水解产物能发生银镜反应 |
在200 mL含Mg2+、Al3+、NH4+、H+、Cl-等离子的溶液中,逐滴加入4mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mol)关系如下图所示。下列叙述正确的是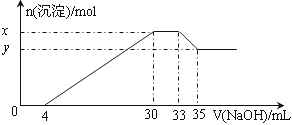
| A.原溶液中n(Mg2+)∶n(Al3+)=10∶1 |
| B.原溶液的c(H+)=0.8 mol/L |
| C.x与y的差值为0.01 mol |
| D.原溶液中c(Cl-)=0.66mol/L |
下列实验报告记录的实验现象正确的是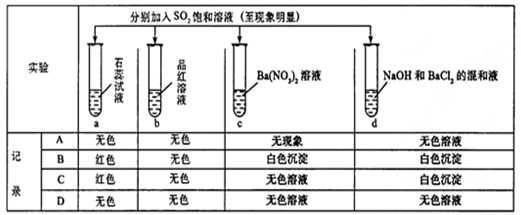
在含有1mol KAl(SO4)2的明矾溶液中滴入含有2mol溶质的Ba(OH)2溶液,充分反应后,当SO42-全部转化为BaSO4沉淀时,铝元素的存在形式是
| A.Al(OH)3和Al3+ | B.Al(OH)3和AlO2- |
| C.Al3+、Al(OH)3和AlO2- | D.全部为AlO2- |