已知下列热化学方程式:
① Fe2O3(s) + 3CO(g) =" 2Fe(s)" + 3CO2(g) △H= -25kJ·mol-1
② 3Fe2O3(s) + CO(g) = 2Fe3O4(s) + CO2(g) △H=" -" 47kJ·mol-1
则下列关于Fe3O4(s)被CO还原成Fe(s)和CO2的热化学方程式的书写中正确的是( )
| A.Fe3O4 + 4CO =" 3Fe" + 4CO2△H= -14kJ·mol-1 |
| B.Fe3O4(s) + 4CO(g) =" 3Fe(s)" + 4CO2(g)△H= -22kJ·mol-1 |
| C.Fe3O4(s) + 4CO(g) =" 3Fe(s)" + 4CO2(g)△H= +14kJ·mol-1 |
| D.Fe3O4(s) + 4CO(g) =" 3Fe(s)" + 4CO2(g)△H= -14kJ·mol-1 |
用水稀释0.1摩/升氨水时,溶液中随着水量的增加而减小的是
A.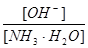 |
B. |
| C.[H+]和[OH-]的乘积 | D.OH-的物质的量 |
向下列溶液滴加稀硫酸,生成白色沉淀,继续滴加稀硫酸,沉淀又溶解的是
| A.Na2SiO3 | B.BaCl2 | C.FeCl3 | D.NaAlO2 |
下列叙述中正确的是()
| A.常温常压下,1 mol羟基(-OH)所含的电子数为10 NA |
| B.由Cu、Zn和稀硫酸组成的原电池工作时,若Cu极生成0.2 g H2,则电路中通过0.2 mol电子 |
| C.在标准状况下,11.2 L NO与11.2 L 02混合后气体分子数为0.75 NA |
| D.l mol Na202,与足量水反应,转移电子的物质的量为2 mol |
下列各组物质依次表示a、b、c、d,满足如图所示转化关系的是(图中箭头表示一步转化)
| A.Si SiO2 Na2SiO3 H2SiO3 |
| B.CH2=CH2 CH3CH2OH CH3CHO CH3COOH |
| C.Fe Fe(NO3)3 Fe(OH)3 Fe2O3 |
| D.Al Al2O3 AlCl3 Al(OH)3 |
如图所示,2个X分子反应生成1个Y分子和3个Z分子,下列判断不正确的是
| A.根据质量守恒定律可推知,1个Z分子中含有2个A原子 |
| B.该反应属于分解反应 |
| C.该反应属于氧化还原反应 |
| D.X、Y、Z三种物质均属于非电解质 |