不管化学反应过程是一步完成还是分为数步完成,这个过程的热效应是相同的。
已知:H2O(g)===H2O(l) ΔH1=-Q1 kJ·mol-1①
C2H5OH(g)===C2H5OH(l) ΔH2=-Q2 kJ·mol-1②
C2H5OH(g)+3O2(g)===2CO2(g)+3H2O(g) ΔH=-Q3 kJ·mol-1③
若使23 g酒精液体完全燃烧,最后恢复到室温,则放出的热量为( )
| A.(Q1+Q2+Q3) kJ | B.[0.5(Q1+Q2+Q3)] kJ |
| C.(0.5Q1-1.5Q2+0.5Q3) kJ | D.(1.5Q1-0.5Q2+0.5Q3) kJ |
在容积不变的密闭容器中存在如下反应:2SO2(g)+O2(g)  2SO3(g) ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
2SO3(g) ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是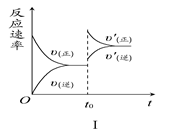
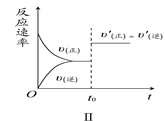

| A.图Ⅰ研究的是t0时刻增大O2的物质的量浓度对反应速率的影响 |
| B.图Ⅱ研究的是t0时刻通入氦气增大体系压强对反应速率的影响 |
| C.图Ⅲ研究的是催化剂对化学平衡的影响,且甲的催化效率比乙高 |
| D.图Ⅲ研究的是温度对化学平衡的影响,且乙的温度较高 |
将4 mol A和2 mol B放入2 L密闭容器中发生反应:2A(g)+B(g)  2C(g) ΔH<0。4 s后反应达到平衡状态,此时测得C的浓度为0.6 mol/L。下列说法正确的是
2C(g) ΔH<0。4 s后反应达到平衡状态,此时测得C的浓度为0.6 mol/L。下列说法正确的是
A.4 s内,v(B)=0.075 mol/(L·s)
B.当c(A)∶c(B)∶c(C)=2∶1∶2时,该反应即达到平衡状态
C.达到平衡状态后,若只升高温度,则C的物质的量浓度增大
D.达到平衡状态后,若温度不变,缩小容器的体积,则A的转化率降低
下列物质中,不能使酸性KMnO4溶液褪色的物质是
①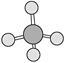 ②乙烯③CH3COOH
②乙烯③CH3COOH
④CH3CH2OH⑤CH2==="CH—COOH" ⑥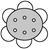
| A.①⑤ | B.①②④⑥ | C.①④ | D.①③⑥ |
下列对非金属元素(除稀有气体元素外)的相关判断正确的是
①非金属元素都是主族元素
②单质在反应中都只能作氧化剂
③氢化物常温下都是气态,所以都叫气态氢化物
④氧化物常温下都可以与水反应生成酸
⑤非金属元素R所形成的含氧酸盐(MaROb)中的R元素必定呈现正价
| A.②⑤ | B.①③⑤ | C.②③④ | D.①⑤ |
下列选项中能发生反应,且甲组为取代反应,乙组为加成反应的是
| 甲 |
乙 |
|
| A |
苯与溴水 |
乙烯与水制乙醇(催化剂) |
| B |
油脂水解(催化剂、加热) |
苯与氢气(催化剂、加热) |
| C |
淀粉水解制葡萄糖(催化剂) |
乙酸和乙醇的酯化反应 (催化剂、加热) |
| D |
乙烯与溴的四氯化碳溶液 |
甲烷与氯气(光照) |