由乙烯和乙醇蒸气组成的混和气体中,若碳元素的质量百分含量为60%,则氧元素的质量百分含量为
| A.15.6% | B.26.7% | C.30% | D.无法确定 |
某物质在酸性条件下可以发生水解反应生成两种物质A、B,且A和B的相对分子质量相等,该物质可能是 ( )
A. 硬脂酸甘油酯 B. 甲酸乙酯(HCOOC2H5)
C.麦芽糖(C12H22O11) D.淀粉〔(C6H10O5)n〕
4进行一氯取代后,只能生成三种沸点不同的有机物的烷烃是( )
C.(CH3)2CHCH(CH3)2 D.(CH3)3CCH2CH3
某有机物的结构简式为: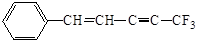 ,则下列说法中不正确的是
,则下列说法中不正确的是
| A.共平面的原子最多有19个 | B.共平面的原子至少有10个 |
| C.共平面的碳原子最多有11个 | D.共直线的碳原子最多有4个 |
白酒、食醋、蔗糖、淀粉均为家庭厨房常用的物质,利用这些物质能完成下列实验的是
①检验自来水中是否含有氯离子②鉴别食盐和小苏打
③蛋壳能否与酸反应④白酒中是否存在甲醇
| A.①② | B.①④ | C.②③ | D.③④ |
下列表示物质结构的化学用语或模型图正确的是
A.CO2的比例模型: 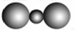 |
B.NH4Cl的电子式为: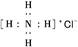 |
| C.丁烷的结构简式CH3(CH2)2CH3 | D.O2-的离子结构示意图: 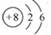 |