某有机化合物A含碳77.8%,氢为7.40%,其余为氧,A的相对分子质量为甲烷的6.75倍。求:
(1)该有机物的分子式。
(2)红外光谱测定,A分子结构中含有苯环和羟基,能与烧碱反应,且在常温下A可与浓溴水反应,1molA最多可与2molBr2作用,据此确定该有机物的结构简式。
我国化工专家侯德榜,勇于创新,改进氨碱法设计了“联合制碱法”,为世界制碱工业作出了突出贡献。请完成下列问题:
(1)“联合制碱法”制得的“碱”是(填化学式)。
(2)氨碱法和联合制碱法是两大重要的工业制碱法,下列表达中,不正确的是。
| 氨碱法 |
联合制碱法 |
||
| A |
原料 |
食盐、氨气、生石灰 |
食盐、氨气、二氧化碳 |
| B |
可能的副产物 |
氯化钙 |
氯化铵 |
| C |
循环物质 |
氨气、二氧化碳 |
氯化钠 |
| D |
评价 |
原料易得;设备复杂;能耗高 |
原料利用率高;废弃物少 |
某实验小组,利用下列装置模拟“联合制碱法”。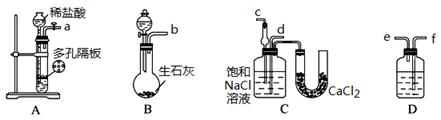
(3)取上述仪器连接装置,顺序为:(a)接()、()接();(b)接();
检验气密性后装入药品,应该先让装置(填上述字母)先发生反应,直到产生的气体不能再在C中溶解时,再通入另一装置中产生的气体。
(4)C中用球形干燥管而不用直导管,其作用是,D中应选用的液体为;
(5)C中广口瓶内产生固体的总化学方程式为。
(6)产品纯碱中含有碳酸氢钠。如果用加热分解的方法测定纯碱中碳酸氢钠的质量分数,纯碱中碳酸氢钠的质量分数可表示为:(注明你的表达式中所用的有关符号的含义)。
某些资料认为:NO、NO2不能与Na2O2反应。某小组学生提出质疑,他们从理论上分析过氧化钠和二氧化氮都有氧化性,根据化合价升降原则提出假设:
假设Ⅰ.过氧化钠氧化二氧化氮
假设Ⅱ.二氧化氮氧化过氧化钠
(1)小组甲同学设计实验如下:
①试管A中反应的化学方程式是。
②待试管B中收集满气体,向试管B中加入适量 Na2O2粉末,塞紧塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将余烬木条迅速伸进试管内,看见木条复燃。甲同学认为假设Ⅱ正确;乙同学认为该装置不能达到实验目的,为达到实验目的,在A、B之间增加一个装置,该装置的作用是。
③乙同学用改进后装置,重复了甲同学的实验操作,观察到红棕色气体迅速消失;余烬木条未复燃。得出结论:假设Ⅰ正确。NO2和Na2O2反应的方程式是。
(2)丙同学认为NO易与O2发生反应,应更易被Na2O2氧化。
查阅资料:① 2NO+Na2O2=2NaNO2
②6NaNO2+3H2SO4=3Na2 SO4+ 2HNO3+4NO↑+2H2O;
③酸性条件下,NO或NO2–都能与MnO4–反应生成NO3–和Mn2+
丙同学用下图所示装置(部分夹持装置略)探究NO与Na2O2的反应。
①B中观察到的主要现象是,F装置的作用是。
②在反应前,打开弹簧夹,通入一段时间N2,目的是。
③充分反应后,检验D装置中发生反应的实验是。
Ullmann(乌尔曼)反应是偶联反应的一种,可以实现卤代苯与含氮杂环的反应。其反应机理如下:
(1)化合物II的分子式为 。
(2)化合物Ⅳ是化合物I的同系物,分子式为C8H9Br,且为苯的对二取代物,其核磁共振氢谱中共有4
组峰,峰的面积之比为3:2:2:2,其所有的结构简式为 、 。
(3)1mol化合物Ⅲ可以与 mol H2发生加成反应;加成后产物的结构简式为 。
(4)化合物Ⅳ的一种同分异构体V的结构简式为 ,V与氢氧化钠的醇溶液在加热条
,V与氢氧化钠的醇溶液在加热条
件下发生的化学反应方程式为 ;反应类型为 。
(5)一定条件下, 与
与 也可以发生Ullmann(乌尔曼)反应,参加反应的物质的量之比为2:1,则生成物的结构简式为 。
也可以发生Ullmann(乌尔曼)反应,参加反应的物质的量之比为2:1,则生成物的结构简式为 。
为了探究AgNO3的热稳定性,某化学兴趣小组设计了如下实验。用如图所示的实验装置A加热AgNO3固体,产生红棕色气体,在装置D中收集到无色气体。当反应结束后,试管中残留固体为黑色。
(1)装置B的作用是。
(2)经小组讨论并验证该无色气体为O2,其验证方法是。
(3)【查阅资料】Ag2O和粉末状的Ag均为黑色;Ag2O可溶于氨水。
【提出设想】试管中残留的黑色固体可能是:ⅰ.Ag;ⅱ.Ag2O;ⅲ.Ag和Ag2O。
【实验验证】该小组为验证上述设想,分别取少量黑色固体放入试管中,进行了如下实验。
| 实验编号 |
操作 |
现象 |
| a |
加入足量氨水,振荡 |
黑色固体不溶解 |
| b |
加入足量稀硝酸,振荡 |
黑色固体溶解,并有气体产生 |
【实验评价】根据上述实验,不能确定固体产物成分的实验是(填实验编号)。
【实验结论】根据上述实验结果,该小组得出AgNO3固体热分解的产物有。
某研究性学习小组设计两套实验方案制备氨气并探究其还原性(部分夹持装置已省略)。
甲方案:如图所示。
乙方案:如图所示。
根据方案回答下列问题:
(一)甲方案
(1)B装置盛装碱石灰,A装置中药品可以是。
a.氯化铵固体和烧碱 b.碳酸氢铵固体
c.氯化铵固体 d.硫酸铵和熟石灰
(2)实验完毕后,设计简单实验检验D试管收集到的物质(简述操作过程、现象和结论)。
(3)写出C中发生反应的化学方程式。
(二)乙方案
(4)A为浓氨水,B为生石灰,简述实验原理:。E装置里盛装的药品是。
(5)能证明氨气具有还原性的实验现象。(任写两条)
(6)铜有+2价、+1价、0价,根据氧化还原反应原理,D玻璃管里还原产物除铜外,还可能有,假设有铜以外的还原产物生成,写出D中发生反应的化学方程式:。