溴化碘(IBr)的化学性质与氯气相似,能跟大多数金属反应生成金属卤化物,能跟水反应:IBr+H2O=HBr+HIO,下列有关叙述中不正确的是( )
| A.IBr是双原子分子 |
| B.在很多化学反应中IBr作氧化剂 |
| C.IBr与水反应时,它既是氧化剂,又是还原剂 |
| D.跟NaOH溶液反应可生成NaI和NaBrO |
FeCl3可用于腐蚀覆有铜箔的绝缘胶板来制作印刷电路板,工业上常采用电解法来处理该反应后的废液。电解时,下列叙述正确的是( )
| A.阳极放出大量氯气 |
| B.阴极放出大量氢气 |
| C.电解液逐渐变为黄色 |
| D.电解液逐渐变为绿色 |
下列电极反应既可以在原电池中发生,又可以在电解池中发生的是()
A.4OH--4e- 2H2O+O2↑ 2H2O+O2↑ |
B.O2+2H2O+4e- 4OH- 4OH- |
C.Cu2++2e- Cu Cu |
D.2H++2e- H2↑ H2↑ |
甲、乙两个电解槽,按图4-19装置进行电解实验,其中a、b、c、d为铂电极,若工作一段时间后,要满足以下条件:①甲池电解液pH升高,乙池电解液pH降低;②b、c两极析出的物质的物质的量相同。下列选项正确的是()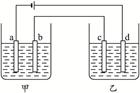
图4-19
| 甲池 |
乙池 |
|
| A |
AgNO3溶液 |
CuCl2溶液 |
| B |
NaOH溶液 |
AgNO3溶液 |
| C |
NaCl溶液 |
CuSO4溶液 |
| D |
H2SO4溶液 |
NaCl溶液 |
铅蓄电池作电源时,正极材料是PbO2,负极材料是Pb,内充稀硫酸,两极总反应为Pb+PbO2+2H2SO4 2PbSO4+2H2O,当电压由2.0 V下降到1.85 V,应停止使用,进行充电,则阴极的电极反应式为( )
2PbSO4+2H2O,当电压由2.0 V下降到1.85 V,应停止使用,进行充电,则阴极的电极反应式为( )
A.PbO2+4H++2e- Pb2++2H2O Pb2++2H2O |
B.Pb-2e- Pb2+ Pb2+ |
C.PbSO4+2e- Pb+SO Pb+SO |
D.PbSO4+2H+-2e- PbO2+4H++SO PbO2+4H++SO |
电解下列熔融物,析出同质量的金属时,消耗电量最少的是()
| A.NaOH |
| B.KCl |
| C.CaCl2 |
| D.Al2O3 |