如右图,利用培养皿探究氨气的性质。实验时向NaOH固体上滴几滴浓氨水,
立即用另一表面皿扣在上面。下列对实验现象所做的解释正确的是
| A.浓盐酸附近产生白烟:NH3与HCl气体反应产生了NH4C1固体 |
| B.浓硫酸附近无明显现象:NH3与浓硫酸不发生反应 |
| C.氯化物溶液变浑浊:该溶液一定是A1Cl3溶液 |
| D.湿润的红色石蕊试纸变蓝:NH3的水溶液显碱性 |
在三个密闭容器中分别充入Ar、H2、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p)从大到小的顺序是
| A.p(H2)>p(O2)>p(Ar) | B.p(O2)>p(Ar )>p(H2) |
| C.p(Ar)>p(H2)>p(O2) | D.p(H2)>p(Ar)>p(O2) |
下列做法中用到物质氧化性的是
| A.铁红做红色颜料 | B.水玻璃做木材防火剂 |
| C.氧化铝做耐火材料 | D.氯气给自来水杀菌、消毒 |
化学无处不在,下列与化学有关的说法不正确的是
| A.侯氏制碱法的工艺过程中应用了物质溶解度的差异 |
| B.硅胶可以除去氯气中的水蒸气 |
| C.明矾净水属于物理变化 |
| D.黑火药由硫黄、硝石、木炭三种物质按一定比例混合制成 |
分析下图所示的四个装置,其中结论正确的是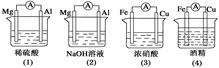
| A.(1)(2)中Mg作负极 |
| B.(3)中Fe作负极,电极反应为Fe-2e-===Fe2+ |
| C.(2)中Mg作正极,电极反应为6H2O+6e-===6OH-+3H2↑ |
| D.(4)中Fe作负极,电极反应为Fe-2e-===Fe2+ |
已知在100℃的温度下(本题涉及的溶液温度均为100℃),水的离子积KW=1×10-12。下列说法正确的是
| A.0.001 mol/L的NaOH溶液pH=9 |
| B.0.1 mol/L的H2SO4溶液pH=1 |
| C.0.005 mol/L的H2SO4溶液与0.01 mol/L的NaOH溶液等体积混合,混合溶液pH为6,溶液显酸性 |
| D.完全中和pH=3的H2SO4溶液50 mL,需要pH=11的NaOH溶液50 mL |