已知25℃时有关弱酸的电离平衡常数:
| 弱酸化学式 |
CH3COOH |
HCN |
H2CO3 |
| 电离平衡常数(25℃) |
1.8×l0_5 |
4.9×l0_10 |
K1=4.3×l0_7 K2=5.6×l0_11 |
则下列有关说法正确的是( )
A.等物质的量浓度的各溶液pH关系为:pH(Na2CO3)>pH(NaCN)>pH(CH3COONa)
B.a mol·L—1 HCN溶液与b mol·L—1 NaOH溶液等体积混合,所得溶液中c(Na+)>c(CN-),则a一定小于b
C.冰醋酸中逐滴加水,则溶液的导电性、醋酸的电离度、pH均先增大后减小
D.NaHCO3和Na2CO3混合溶液中,一定有c(Na+)+ c(H+)=c(OH-)+ c(HCO3-) +2c(CO32-)
在不同条件下分别测得反应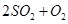

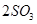 的化学反应速率,其中表示该反应进行得最快的是( )
的化学反应速率,其中表示该反应进行得最快的是( )
A.v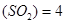 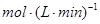 |
B.v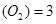 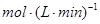 |
C.v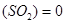 .1 .1 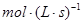 |
D.v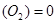 .1 .1 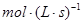 |
在2 L的密闭容器中,发生反应3A(g)+B(g)  2C(g),若最初加入的A和B都是4 mol,测得10 s内A的平均速率v(A)=0.12
2C(g),若最初加入的A和B都是4 mol,测得10 s内A的平均速率v(A)=0.12 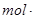
 则反应进行到10 s时容器中B的物质的量是( )
则反应进行到10 s时容器中B的物质的量是( )
A.1.6 mol
B.2.8 mol
C.3.2 mol
D.3.6 mol
在298 K、100 kPa时,已知: 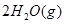 ===
===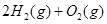

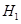
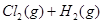 ===2HCl(g)
===2HCl(g)
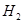
 ===
===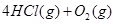


则
 与
与
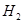 和
和
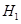 之间的关系正确的是( )
之间的关系正确的是( )
A.  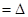 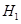  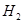 |
B.  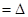 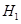  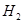 |
C.  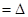 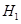  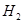 |
D.  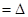 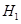 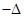 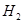 |
可逆反应mA(g) nB(g)+pC(s) ΔH=Q,温度和压强的变化对正、逆反应速率的影响分别符合下图中的两个图象,以下叙述正确的是( )
nB(g)+pC(s) ΔH=Q,温度和压强的变化对正、逆反应速率的影响分别符合下图中的两个图象,以下叙述正确的是( ) 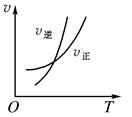
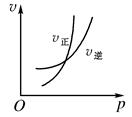
| A.m>n,Q>0 | B.m>n+p,Q>0 | C.m>n,Q<0 | D.m<n+p,Q<0 |
已知下列热化学方程式: 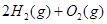 ===
===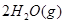
 H="-483.6"
H="-483.6" 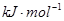
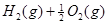 ===
===
 H="-241.8"
H="-241.8" 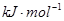
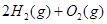 ===
===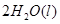
 H="-571.6"
H="-571.6" 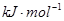
则氢气的燃烧热是( )
A.-483.6 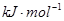 |
B.-241.8 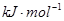 |
C.571.6 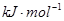 |
D.285.8 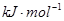 |