哈伯因发明了由氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖。现向一密闭容器中充入1 mol N2和3 mol H2,在一定条件下使该反应发生。下列有关说法正确的是
| A.达到化学平衡时,N2将完全转化为NH3 |
| B.达到化学平衡时,N2、H2和NH3的物质的量浓度一定相等 |
| C.达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化 |
| D.达到化学平衡时,正反应和逆反应的速率都为零 |
化学与日常生活密切相关,下列说法错误的是
| A.碘酒是指单质碘的乙醇溶液 |
| B.“84”消毒液的有效成分是NaClO |
| C.浓硫酸可刻蚀石英制艺术品 |
| D.装饰材料释放的甲醛会造成污染 |
常温下,下列说法不正确的是
| A.0.1 mol/L的Na2SO3溶液中粒子浓度关系:c(OH-)=c(HSO3-)+2c(H2SO3)+c(H+) |
| B.将常温下pH=12的氢氧化钠溶液与pH=2的硫酸溶液分别加热,溶液pH都减小 |
| C.把等体积的1×10-5 mol/L的硫酸与4×10-5 mol/L的NaOH溶液相混合,混合液的pH值与5×10-6 mol/L的Ba(OH)2溶液的pH值相同 |
| D.0.2 mol·L-1CH3COOH溶液与0.1 mol·L-1NaOH溶液等体积混合:2c(H+)-2c(OH-)=c(CH3COO-)-c(CH3COOH) |
Fe2O3、ZnO、CuO的固体混合粉末ag,在加热条件下用足量CO还原,得到金属混合物4.82g,将生成的CO2气体用足量的澄清石灰水吸收后,产生l0.00g白色沉淀,则a 的数值为
| A.6.42 | B.4.92 | C.7.18 | D.14.82 |
乙烯催化氧化成乙醛可设计成如下图所示的燃料电池,能在制备乙醛的同时获得电能,其总反应为:2CH2=CH2 + O2→2CH3CHO。下列有关说法正确的是
| A.该电池为可充电电池 |
| B.每有0.1mol O2反应,则迁移H+ 0.4mol |
| C.正极反应式为:CH2=CH2-2e- + 2OH-→CH3CHO + H2O |
| D.电子移动方向:电极a→磷酸溶液→电极b |
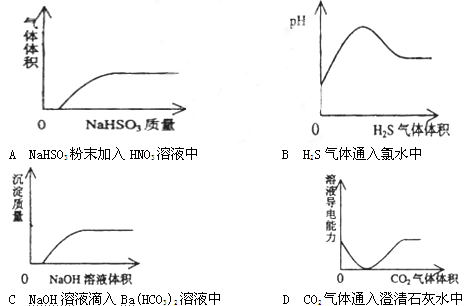
下列实验过程中产生的现象与对应的图形相符合的是