下列反应的离子方程式正确的是
| A.用醋酸除去水垢:CaCO3 + 2H+=Ca2+ + H2O + CO2↑ |
| B.利用腐蚀法制作印刷线路板:Fe3+ + Cu = Fe2+ + Cu2+ |
| C.次氯酸钙溶液中通入过量二氧化硫:Ca2++2Cl0一+S02+H20=CaSO3↓+2HClO |
| D.等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合: |
Ba2++20H-+NH4++HCO3-=BaC03↓+NH3·H2O+H20
在同温同压下,下列各组热化学方程式中 Q1 <Q2的是(反应条件已略去)
| A.2H2(g) + O2(g) = 2H2O(g) ;△H=-Q1 , 2H2(g) + O2(g) = 2H2O(l) ;△H=-Q2 |
| B.S(g) + O2(g) = SO2(g) ;△H=-Q1 , S(s) + O2(g) = SO2(g) ;△H=-Q2 |
| C.C(s) + 1/2O2(g) =" CO(g)" ;△H=-Q1 , C(s) + O2(g) = CO2(g) ;△H=-Q2 |
| D.H2(g) + Cl2(g) =" 2HCl(g)" ;△H=-Q1 , 1/2H2(g) + 1/2Cl2(g) =" HCl(g)" ;△H=-Q2 |
将浓度为0.1mol·L-1HF溶液加水不断稀释,下列各量始终保持增大的是
| A. c(H+) | B.Ka(HF) | C.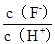 |
D. |
下列液体均处于25℃,有关叙述正确的是
| A.某物质的溶液pH < 7,则该物质一定是酸或强酸弱碱盐 |
| B.pH= 4.5的番茄汁中c(H+)是pH= 6.5的牛奶中c(H+)的100倍 |
| C.AgCl在同浓度的CaCl2和NaCl溶液中的溶解度相同 |
| D.pH= 5.6的CH3COOH与CH3COONa混合溶液中,c(Na+) > c(CH3COO-) |
某温度下,Fe(OH)3(s)、Cu(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液pH,金属阳离子浓度的变化如图所示。据图分析,下列判断错误的是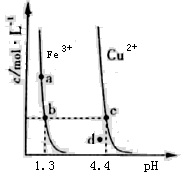
| A.Ksp<Ksp2 |
| B.加适量NH4Cl固体可使溶液由a点变到b点 |
| C.c、d两点代表的溶液中c(H+)与c(OH-)乘积相等 |
| D.Fe(OH)3、Cu(OH)2分别在b、c两点代表的溶液中达到饱和 |
下列与化学反应能量变化相关的叙述正确的是
| A.生成物总能量一定低于反应物总能量 |
| B.放热反应的反应速率总是大于吸热反应的反应速率 |
| C.应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| D.同温同压下,H2(g)+Cl2(g) |