相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:
2 SO2(g)+O2 (g) 2SO3(g) △H=-196.4 kJ/mol。
2SO3(g) △H=-196.4 kJ/mol。
实验测得起始、平衡时的有关数据如下表:
| 容器编号 |
起始时各物质物质的量/mol |
平衡时反应中的能量变化 |
||
| SO2 |
O2 |
SO3 |
||
| ① |
2 |
1 |
0 |
放出热量a kJ |
| ② |
1 |
0.5 |
1 |
放出热量b kJ |
| ③ |
4 |
2 |
0 |
放出热量c kJ |
下列叙述正确的是
A.放出热量关系:a = b B.三个容器内反应的平衡常数:③>②>①
C.平衡时SO3气体的体积分数:③>① D.SO2的转化率:②>①>③
下列有关原子结构及元素周期律的叙述正确的是( )。
| A.同主族元素的原子最外层电子数相同,化学性质也相同 |
| B.同周期元素(除0族元素外)从左到右,原子半径逐渐减小 |
| C.第ⅦA族元素从上到下,其氢化物的稳定性逐渐增强 |
| D.同主族元素从上到下,单质的熔点逐渐降低 |
下表是元素周期表的一部分,有关说法正确的是( )。
| 族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
| 2 |
a |
b |
|||||
| 3 |
c |
d |
e |
f |
①a、b、c、d四种元素的原子半径:d>c>b>a
②六种元素中金属性最强的是c
③a、f两种元素氢化物的稳定性:f>a
④a、b、f三种元素最高价氧化物对应的水化物的酸性最强的是b
A.③④ B.②③ C.②④D.①③
X、Y、Z是位于不同周期的三种短周期元素,且原子序数逐渐增大,X、Z位于同一主族,三种元素可以形成原子个数比为1∶1∶1的化合物W。下列推测正确的是( )。
| A.元素Z的氧化物一定属于碱性氧化物 |
| B.原子半径:X<Y<Z |
| C.三种元素中,Y的金属性最强 |
| D.Y、Z都能形成含氧酸,且前者的酸性比后者强 |
下列说法正确的是( )。
| A.金属元素和非金属元素间形成的化学键一定是离子键 |
| B.ⅦA族元素是同周期元素中非金属性最强的元素 |
| C.全部由非金属元素形成的化合物一定是共价化合物 |
| D.短周期中,同周期元素的离子半径从左到右逐渐减小 |
下列关于指定粒子构成的叙述中,不正确的是( )。
| A.37Cl与39K具有相同的中子数 |
B.第114号元素的一种核素 与 与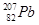 具有相同的最外层电子数 具有相同的最外层电子数 |
| C.H3O+与OH-具有相同的质子数和电子数 |
| D.O22-与S2-具有相同的质子数和电子数 |