某研究性学习小组为证明2Fe3+ + 2I-  2Fe2+ + I2为可逆反应(即反应存在一定的限度),设计如下几种方案。已知FeF63-是一种无色的稳定的络离子。
2Fe2+ + I2为可逆反应(即反应存在一定的限度),设计如下几种方案。已知FeF63-是一种无色的稳定的络离子。
按要求回答下列问题。
方案甲:
取5mL 0.1mol/L KI溶液,滴加2ml 0.1mol/L 的FeCl3溶液,再继续加入2mL CCl4,充分振荡。静置、分层,再取上层清液,滴加KSCN溶液。
(1)甲方案中能证明该反应为可逆反应的现象是 。
(2)有同学认为该方案设计不够严密,即使该反应为不可逆反应也可能出现上述现象,其原因是 。
方案乙:
取5mL 0.1mol/L KI溶液,滴加2ml 0.1mol/L 的FeCl3溶液,溶液呈棕黄色,再往溶液中滴加NH4F溶液,若看到 现象,即可证明该反应为可逆反应,请解释产生该现象的原因 。
方案丙:
设计如图原电池装置,接通灵敏电流计,指针向右偏转(注:灵敏电流计指针总是偏向电源正极),随着时间进行电流计读数逐渐变小,最后读数变为零。
当指针读数变零后,在乙烧杯中加入1mol/L FeCl2溶液,若观察到灵敏电流计的指针向 方向偏转(填“左”、“右”或“不移动”),即可判断该反应为可逆反应,此时甲中石墨电极上的电极反应式为 。
某课外小组设计的实验室制取乙酸乙酯的装置如下图所示,A中放有浓硫酸,B中放有乙醇(含18O)、无水醋酸钠,D中放有含有酚酞饱和碳酸钠溶液。
已知①无水氯化钙可与乙醇形成难溶于水的CaCl2·6 C2H5OH ; ②有关有机物的沸点:
| 试剂 |
乙醚 |
乙醇 |
乙酸 |
乙酸乙酯 |
| 沸点/℃ |
34.7 |
78.5 |
118 |
77.1 |
请回答:
(1)浓硫酸的作用是;若用同位素180示踪法确定反应产物水分子中氧原子的提供者,写出能表示18O位置的化学方程式:。
(2)球形干燥管C的作用是。反应结束后D中的现象是。
(3)上述实验中饱和碳酸钠溶液的作用是。
(4)欲从D中得到乙酸乙酯的分离方法是;从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出;
(5)某化学课外小组设计了如图所示的制取乙酸乙酯的装置(图中的铁架台、铁夹、加热装置已略去),与上图装置相比,此装置的主要优点有:(请写出两点)
,。 
(共14分)某同学设计如下实验装置探究硫酸与金属、非金属的反应、验证其产物,并探究随着反应的进行,硫酸性质发生的变化。根据实验要求回答相关问题:
F装置用于检验二氧化碳。供选择的试剂有:只含碳的生铁、18 mol·L-1的硫酸、品红溶液、无水硫酸铜粉未、酸性高锰酸钾溶液、氧化铜、澄清的石灰水、碱石灰。(供选择的试剂可重复使用)
(1)打开分液漏斗的活塞,A装置中发生的反应6H2SO4(浓)+2Fe Fe2(SO4)3+6H2O↑+3SO2↑和(用化学方程式表示),随反应的进行,硫酸的浓度变稀,又发生反应(用化学方程式表示)。
Fe2(SO4)3+6H2O↑+3SO2↑和(用化学方程式表示),随反应的进行,硫酸的浓度变稀,又发生反应(用化学方程式表示)。
(2)B装置中的试剂是。
(3)E装置中的作用是。
(4)G装置中的试剂是,现象是。
(5)从安全角度考虑,应后点燃的酒精灯(填“A”或“G”)。你认为本实验尾气是否需要处理?(填“是”或“否”),如需处理,具体方案是。
某学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
| 时间(min) |
1 |
2 |
3 |
4 |
5 |
| 氢气体积(mL) |
50 |
120 |
232 |
290 |
310 |
(1)哪一时间段(指0~1、1~2、2~3、3~4、4~5 min)反应速率最大,原因是。
(2)哪一段时段的反应速率最小,原因是。
(3)求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率(设溶液体积不变,要写出计算过程)。
(4)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液:你认为可行的是(填编号) 。
A.蒸馏水 B.NaCl溶液 C.Na2CO3溶液 D.CuSO4溶液
溴乙烷是一种重要的有机化工原料,其沸点为38.4℃。制备溴乙烷的一种方法是乙醇与氢溴酸反应.某课外小组欲在实验室制备溴乙烷的装置如图,实验操怍步骤如下: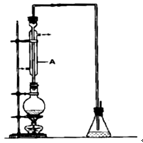
①检查装置的气密性;
②在圆底烧瓶中加入95%乙醇、溴化钠、浓硫酸及几粒碎瓷片;
③小心加热,使其充分反应。
请问答下列问题。
(1)装置A的作用是。
(2)反应结束后,得到的粗产品呈棕黄色(含少量的溴单质)。为了除去粗产品中的杂质,可选择下列试剂中的(填写上正确选项的字母)。
a.亚硫酸钠溶液b.氢氧化钠溶液
c.乙醇d.四氯化碳
该实验操作中所需的主要玻璃仪器是(填仪器名称)。
(3)要进一步制得纯净的溴乙烷,可继续用蒸馏水洗涤,分液后,再加入无水 ,然后进行的实验操作是(填写正确选项的字母)。
,然后进行的实验操作是(填写正确选项的字母)。
a.分液b.蒸馏 c.萃取
(4)为了检验溴乙烷中含有溴元素,通常采用的方法是取少量溴乙烷,然后(按实验的操作顺序选填下列序号)。
①加热 ②加入 溶液③加入稀
溶液③加入稀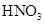 酸化④加入NaOH溶液
酸化④加入NaOH溶液
实验室常用二氧化锰和浓盐酸反应制备氯气,用下图装置可制备纯净、干燥的氯气,并验证其部分性质。
试回答下列问题:
(1)A中发生反应的化学方程式是。
(2)C、D中所用试剂分别是:C;D。
(3)B中出现的现象是。
(4)请用离子方程式表示F中NaOH溶液的作用。
(5)若想制得标准状况下2.24L氯气,理论上被氧化的HCl的物质的量是mol。