下列实验用来证明SO2的存在,其中正确的是( )
| A.能使品红褪色。 |
| B.能使湿润的蓝色石蕊试纸变红。 |
| C.通入足量的NaOH溶液中,再滴入BaCl2溶液有白色沉淀生成,该沉淀溶于稀盐酸。 |
| D.通入稀溴水中能使溴水褪色,得澄清溶液,再滴加Ba(NO3)2溶液有白色沉淀,该沉淀不溶于硝酸。 |
下列表示化学反应的离子方程式正确的是
| A.Na2O2与水反应:Na2O2 + H2O = 2Na+ + 2OH- + O2↑ |
B.用惰性电极电解MgCl2溶液:2Cl-+2H2O 2OH-+H2↑+Cl2↑ 2OH-+H2↑+Cl2↑ |
| C.Ba(OH)2溶液中加入过量的NaHSO4溶液:Ba2++SO42-+OH-+H+=BaSO4↓+H2O |
| D.硫酸亚铁溶液中加入酸化的双氧水:2Fe2++2H++H2O2=2Fe3++2H2O |
下列离子在给定的条件下一定能大量共存的是
| A.加入Al粉放出H2的溶液中:Na+、K+、Fe3+、NO3— |
| B.c(Fe3+)=0.1mol/L的溶液中:NH4+、Cl—、AlO2—、SO42— |
| C.水电离出的c(H+)=1×10-13mol/L的溶液中:Mg2+、K+、NO3—、Cl— |
| D.含有SCN—离子的溶液中:Ca2+、Fe2+、NO3—、Cl— |
生活中遇到的某些问题,常常涉及到化学知识,下列各项叙述正确的是
| A.“加碘盐”、“高钙牛奶”、“富硒营养品”等食用品中的碘、钙、硒是指单质 |
| B.铝合金的大量使用归功于人们能用焦炭等还原剂从氧化铝中获取铝单质 |
| C.医疗上进行胃部造影前,患者服用的“钡餐”是BaCO3等不溶于水的物质 |
| D.“酸可以除锈”、“热的纯碱溶液去油污”,都发生了化学变化 |
下列有关化学用语表示正确的是
A.钾原子结构示意图: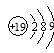 |
B.水的电子式: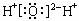 |
C.CO2的比例模型: |
D.间羟基苯甲酸的结构简式: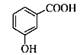 |
下列实验操作与预期实验目的或所得实验结论一致的是
| 选项 |
实验操作 |
实验目的或结论 |
| A |
向苯中滴入少量浓溴水,振荡,静置 |
溶液分层,上层呈橙红色,下层几乎无色,苯和溴水发生取代反应,使溴水褪色 |
| B |
向含有少量FeCl3的MgCl2溶液中加入足量Mg(OH)2粉末,搅拌一段时间后过滤 |
除去MgCl2溶液中少量FeCl3 |
| C |
向鸡蛋清溶液中加入饱和(NH4)2SO4溶液 |
有白色沉淀产生,蛋白质发生了变性 |
| D |
C2H5OH与浓硫酸170 ℃共热,制得的气体通入酸性KMnO4溶液 |
检验制得气体是否为乙烯 |