下表是元素周期表的一部分,列出了七种元素的周期表中的位置:
| |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
| 2 |
|
|
|
① |
|
② |
③ |
| 3 |
④ |
⑤ |
⑥ |
|
|
|
⑦ |
请用化学符号按要求回答下列问题:
(1)这七种元素中,非金属性最强的是 ,在元素周期表中的位置
(2)元素①与②形成摩尔质量为44g /mol的物质,它的电子式是
(3)③、⑥、⑦三种元素的原子半径由大到小的顺序是 。
(4)④元素最高价氧化物对应的水化物与⑥元素的最高价氧化物对应的水化物反应的化学反应方程式是
(5)④、⑤、⑥三种元素最高价氧化物的水化物碱性强弱顺序是
(11分)四种元素X、Y、Z、W位于元素周期表的前四周期,已知它们的核电荷数依次增加,且核电荷数之和为51;Y原子的L层p轨道中有2个电子;Z原子与Y原子的价层电子数相同;W原子的L层电子数与最外层电子数之比为4:1,其d轨道中的电子数与最外层电子数之比为5:1。
(1)Y、Z可分别与X形成只含一个中心原子的共价化合物a、b,a的分子式是_____,b的结构式是_______;中心原子的杂化轨道类型分别是________、_________;a分子的立体结构是____________;
(2)Y的最高价氧化物和Z的最高价氧化物的晶体类型分别是_______晶体、_______晶体;
(3)X的氧化物与Y的氧化物中,分子极性较小的是(填分子式);
(4)Y与Z比较,电负性较大的是____________;
(5)W的元素符号是,其+2价离子的核外电子排布式是
(12分)根据要求完成下列问题:
(1)分析下列物质的物理性质,判断其晶体类型:
A、固态时能导电,能溶于盐酸;B、能溶于CS2,不溶于水;C、固态、液态时均不导电,熔点3500℃
A、B、C、
(2)指出配合物K3[Co(CN)6]中的中心离子、配体及其配位数:_________、__________、_________。
(3)在H2、SiC、CO2、HF中,由极性键组成的非极性分子是,由非极性键形成的非极性分子是,能形成分子晶体的化合物是,含有氢键的晶体的化学式,属于原子晶体的是,四种物质熔点由高到低的顺序是。
河道旁有甲、乙两厂。它们排放废水中含K+、Ag+、Fe3+、C1-、OH-、NO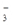 六种离子。
六种离子。
(1)甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子是、、。
(2)乙厂的废水中含有另外三种离子。如果加一定量(选填“活性炭”“铁粉”),可以回收其中的。
医学上常用酸性高锰酸钾溶液和草酸溶液的反应用于测定血钙的含量。回答下列问题:
H++MnO4-+H2C2O4→CO2↑+Mn2++
(1)配平以上离子方程式,并在□中填上所需的微粒。(2)该反应中的还原剂是。
(3)反应转移了0.4mol电子,则消耗KMnO4的物质的量为mol。
【化学—有机化学基础】(13分)
奶油中含有有一种可作香料的化合物A,A中只含C、H、O三种元素。通过红外光谱图分析可知A中含有碳氧双键;通过李比希法分析得到A分子中C、H、O原子个数比为2:4:1,通过质谱仪分析其相对分子质量为88。
已知: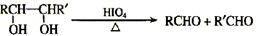
与A相关的反应如下: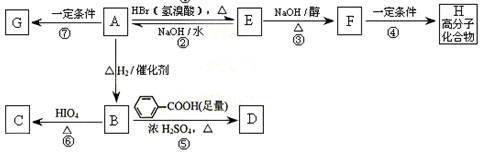
(1)A的分子式为,H的结构简式为。
(2)上述7步反应中属于取代反应的是(填序号)。
(3)写出B → D反应的化学方程式:。
(4)B的核磁共振氢谱图中共有个峰。
(5)在空气中长时间搅拌奶油,A可转化为相对分子质量为86的化合物G。G有多种同分异构体,其中符合下列两个条件的同分异构体共有种。
A.无环状结构B.不含碳碳双键和碳碳叁键