(7分)小明在查阅资料时得知CO2在高温时能与木炭反应生成CO ,他决定对该反应进行探究。
【提出问题】CO2与木炭在高温条件下反应是否生成CO?
【实验探究】小明设计了下图的实验方案,并进行实验。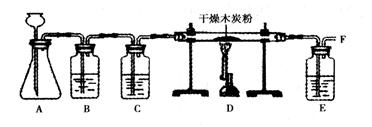
A中用石灰石与稀盐酸反应的化学方程式为___________________。
检查装置A气密性的方法是__________________________________________
B中装有饱和碳酸氢钠溶液,其作用是除去CO2气体中混有的少量HCl气体。C中装有浓硫酸,其作用是__________________
E中氢氧化钠溶液的作用是__________________。
【实验结论】经检验F处的气体为CO。结论:CO2在高温条件下与木炭反应生成了CO。
【实验反思】
有同学对A装置作如下改进:在锥形瓶中放入一小试管,将长颈漏斗下端插入小试管中,改进后的优点是_________________。
【实验拓展】
撤去B,按A→C→D→E顺序连接。然后A中用二氧化锰和过氧化氢溶液混合生成O2,反应的化学方程式为_________________。此时要检验该实验条件下D中木炭所发生反应的所有生成物,除在F处点燃并检验生成物外,还需要补充和完善的实验是________________。
铝制品在日常生活中应用广泛,但铝制品却不宜长时间盛放腌制食品。资料显示:“铝制品表面虽然有一层致密的氧化膜保护……氯化钠也会破坏氧化膜的结构,加速铝制品的腐蚀。”
【提出问题】氯化钠溶液中的哪一种离子对氧化膜产生了破坏作用?
【实验方案】
【反思】针对实验3,莹莹认为还应增做一个对比实验,她的方案是向B试管中再加入Na2SO4溶液,结果无明显现象。该实验可证明溶液中对氧化膜不产生破坏作用的离子是____。
【定量计算】现有一块表面被氧化的铝片4克,放入到100克足量的稀盐酸溶液的烧杯中,待固体完全消失后,称得烧杯中剩余物的总质量为l03.7克,求该铝片中氧化铝的质量。
某研究性学习小组在验证“碱使酚酞试液变红”的实验时,发现一个意外现象:将酚酞试液滴人某NaOH溶液中,溶液变成了红色,可是过一会儿红色却消失了。
【提出问题】是什么原因导致滴有酚酞的NaOH溶液由红色褪为无色?
【猜想与假设】他们分别对这种意外现象作如下猜想:
甲同学:可能是酚酞与O2发生了反应;
乙同学:可能是NaOH溶液与空气中的CO2发生了反应;
丙同学:可能与NaOH溶液浓度大小有关;
你认为可能还与_________________________________有关(写一条即可)。
【设计实验】三位同学分别设计实验验证自己的猜想:
(1)甲同学设计了如下实验,请你填写下表。
| 实验步骤 |
设计这一步骤的目的 |
实验现象 |
实验结论 |
| 1.将NaOH溶液加热煮沸 |
溶液变红,过一会儿红色消失 |
甲同学猜想___________(填“正确”或不正确”) |
|
| 2.向冷却后的溶液中滴人酚酞,并滴一些植物油在其上方 |
(2)乙同学设计如图装置进行实验,一段时间后,试管中溶液的红色褪去,于是认定自己的猜想正确。请写出CO2与NaOH溶液反应的化学方程式:________________________。甲同学认为乙同学的实验不够严谨,理由是________________________。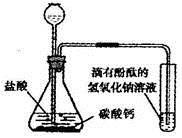
(3)丙同学使用了色度传感器测溶液的颜色。他在a、b、c三个比色皿中分别加入等量5%、10%、20%的NaOH1溶液,然后各滴加2滴酚酞试液。溶液颜色的变化曲线如图[说明:溶液无色时色度值(透过率)为100%]。请你观察下图回答问题。①写出两条规律性结论:___________________________________________________;
___________________________________________________。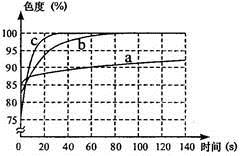
②推测5%的NaOH溶液滴加2滴酚酞试液后褪为无色的时间约为
A.小于30s
B.30-90s
C.90-140s
D.140-180s
E.180-280s
F.大于280s
红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如下图所示.同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究.
| 品名:504双吸剂 成分:铁粉、生石灰等 |
【提出问题】久置固体的成分是什么?
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.久置固体中可能含有Ca(OH)2的原因是(用化学方程式表示).
【实验探究1】
甲同学的方案:
| 实验操作 |
实验现象 |
实验结论 |
| (1)取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液 |
固体溶解时试管外壁发烫,试管底部有不容物,溶液变红. |
固体中一定含有 和氢氧化钙. |
| (2)另取少量固体放于试管中,滴加足量的. |
固体逐渐消失,有大量无色气体产生,得到浅绿色溶液. |
固体中一定含有, 一定不含Fe2O3 |
| (3)将步骤(2)中产生的气体通入到澄清的石灰水中 |
固体中一定含有CaCO3 |
【实验质疑】
(1)乙同学认为甲同学的实验中不能得出一定含Ca(OH)2的结论,理由是.
(2)丙同学认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是.
【实验探究2】
乙、丙同学设计如下实验方案继续验证:
(1)③中反应的化学方程式是.
(2)乙、丙同学实验中又能得出固体样品中一定还含有,仍有一种物质不能确定,该物质是.
(3)乙、丙同学又经过实验测得上述残留固体中含钙物质的总质量为1.6g,滤渣B中CaCO3的质量为1.0g,滤渣C的质量为1.0g.
【实验结论】综合上述实验及所给数据,久置固体的成分是.
老师在装有酸的储物柜中发现一瓶没有标签的溶液,让同学们鉴定该溶液是否为盐酸溶液。
| 实验步骤 |
实验现象 |
实验结论 |
| 1.取少量待测液体与试管中,滴加几滴石蕊溶液 |
溶液呈酸性 |
|
| 2.取少量待测液与试管中,滴加 溶液 |
产生了白色沉淀 |
该待测溶液为盐酸 |
| 3.往上述2中的沉淀滴加 溶液 |
写出上述操作2中所发生的化学方程式:。
化学兴趣小组的同学对一份固体样品进行了探究。通过实验已确定该样品由氧化铁和铁粉混合而成。为进一步探究各成分的含量,他们称取了13.6g固体样品,用图1所示的装置继续实验,测定的部分数据如图2所示。
【实验步骤】
(1)按上图连接装置,并检查装置气密性。称取13.6g样品,放入硬质玻璃管中;
(2)先通一段时间CO,再点燃酒精喷灯;
(3)待反应结束,熄灭酒精喷灯,再缓缓同入一段时间CO;
(4)冷却至室温,称取硬质玻璃管中固体质量
(5)测定澄清石灰水较反应前增重4.4g
反应前先通CO的目的;硬质玻璃管中发生反应的化学方程式;广口瓶中观察到的现象。
【数据处理】
请你根据有关数据,计算样品中氧化铁的质量分数。(请在答题纸上写出完整的解题步骤)
【问题讨论】
(1)有同学不赞同使用步骤(5)中的数据,原因是。
(2)从环境保护的角度,请你提出一个实验改进的措施。