如图所示,隔板I固定不动,活塞Ⅱ可自由移动,M、N两个容器中均发生反应:A(g) + 3B(g)  2C(g) ΔH="-192" kJ·mol-1。向M、N中,都通入x mol A和y mol B的混合气体,初始M、N容积相同,保持温度不变。下列说法正确的是
2C(g) ΔH="-192" kJ·mol-1。向M、N中,都通入x mol A和y mol B的混合气体,初始M、N容积相同,保持温度不变。下列说法正确的是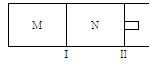
| A.若平衡时A气体在两容器中的体积分数相等,则x一定等于y |
| B.若x∶y=1∶2,则平衡时,M中的转化率:A>B |
| C.若x∶y=1∶3,当M中放出热量172.8 kJ时,A的转化率为90% |
| D.若x=1.2,y=1,N中达到平衡时体积为2 L,含有C 0.4 mol,再通入0.36 mol A时,v(正)<v(逆) |
对A +3B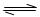 2C +2D来说,下列四种不同情况下的反应速率最快的是
2C +2D来说,下列四种不同情况下的反应速率最快的是
A.υ(A)=" 0.15" mol·(L·min)-1 B.υ(B)=" 0.6" mol·(L·min)-1
C.υ(C)=" 0.4" mol·(L·min)-1 D.υ(D)=" 0.45" mol·(L·min)-1
下列说法正确的是
| A.水解反应是吸热反应 | B.升高温度可以抑制盐类的水解 |
| C.正盐水溶液pH均为7 | D.硫酸钠水溶液pH小于7 |
下列说法正确的是
| A.凡是放热反应都是自发的。 | B.铁在潮湿空气中生锈是自发过程 |
| C.自发反应都是熵增大的反应。 | D.电解池的反应是属于自发反应 |
下列说法不正确的是
| A.反应物和生成物所具有的总能量的差决定了化学反应是放热还是吸热 |
| B.当化学反应A→B △H <O,则稳定性B>A |
| C.△H近似等于生成物的总键能减去反应物的总键能 |
| D.吸热反应在常温、常压下也可能发生 |
化学反应过程中发生物质变化时,常常伴有能量的变化。这种能量的变化常以热能的形式表现出来,叫反应热。由于反应的情况不同,反应热可以分为多种,如标准燃烧热和中和热等等。下列△H表示标准燃烧热的是
| A.2H2(g)+O2(g)===2H2O(l);△H1 |
| B.C(s)+1/2O2(g)===CO(g);△H2 |
| C.4NH3(g)+5O2(g)===4NO(g)+6H2O(l);△H3 |
| D.C(s)+O2(g)===CO2(g);△H4 |