如图所示,杠杆AB两端分别持有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向烧杯中央滴入较浓的硫酸铜溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中不考虑两球的浮力变化):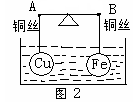
| A.当杠杆为绝缘体时,A端高、B端低;为导体时,A端低、B端高 |
| B.当杠杆为绝缘体时,A端低、B端高;为导体时,A端高、B端低 |
| C.当杠杆为导体或绝缘体时,均为A端高B端低 |
| D.当杠杆为导体或绝缘体时,均为A端低B端高 |
用固体NaOH配制一定物质的量浓度的NaOH溶液,下列操作正确的是
| A.称量时,将固体NaOH放在小烧杯中,再放在天平左盘上 |
| B.将称量好的固体NaOH放入容量瓶中,加蒸馏水溶解 |
| C.定容时如果加水超过了刻度线,用胶头滴管直接吸出多余部分 |
| D.将烧杯中溶解固体NaOH所得溶液,冷却到室温后转移至容量瓶中 |
下列有关物质分离方法的叙述中,正确的是
| A.用酒精萃取碘水中的碘 |
| B.用蒸馏的方法将自来水制成蒸馏水 |
| C.用蒸发食盐水的方法得到氯化钠晶体 |
| D.用过滤的方法分离二氧化硅和氧化钙的混合物 |
下列实验现象与对应化学方程式都正确的是
| A.金属钠投入水中,浮在水面熔成小球,并在水面快速移动,得到的溶液显碱性; 2 Na + 2 H2O  2 NaOH+ H2↑ 2 NaOH+ H2↑ |
| B.氢气在氯气中安静的燃烧,发出淡蓝色火焰,瓶口出现白雾;H2 + Cl2 2HCl |
C.FeSO4溶液中加入NaOH溶液时,生成的白色絮状沉淀迅速变为灰绿色,最后变成红褐色; 2Fe(OH)2 + O2 + H2O  2 Fe(OH)3 2 Fe(OH)3 |
| D.向Na2SiO3溶液中逐滴加入稀盐酸,边加边振荡,有透明的硅酸凝胶产生; |
Na2SiO3+ 2HCl  H2SiO3(胶体) + 2NaCl
H2SiO3(胶体) + 2NaCl
下列化学方程式改写成离子方程式正确的是
| A.2NaOH + Cl2=" NaCl" + NaClO + H2O ; Cl2+ 2OH-= Cl-+ ClO-+ H2O |
| B.CaCO3 + 2HCl =CaCl2+ CO2 + H2O; CO32- + 2H+ = CO2 + H2O |
| C.Al2(SO4)3 +6NH3·H2O =" 2" Al(OH)3↓+3 (NH4)2SO4; Al3+ + 3NH3·H2O = Al(OH)3↓ + 3 NH4+ |
| D.Ba(OH)2+H2SO4 = BaSO4 ¯+2H2O; 2H+ +2OH- = 2H2O |
NA代表阿伏加德罗常数,下列说法正确的是
| A.1 mol NaCl固体溶于1 L水所得溶液中NaCl的物质的量浓度为1 mol·L-1 |
| B.5.6 g铁在足量氯气中燃烧时失去的电子数目为0.3NA |
| C.常温常压下,11.2 L H2所含的分子数目为0.5NA |
| D.17g氨气所含的质子数目为10 NA |