在标准状况下有①6.72L CH4,②3.01 1023个HCl分子,③13.6gH2S,④0.2mol氨气。下列对这四种气体的关系从大到小描述不正确的是
1023个HCl分子,③13.6gH2S,④0.2mol氨气。下列对这四种气体的关系从大到小描述不正确的是
| A.体积:②>③>①>④ |
| B.氢原子数:①>④>③>② |
| C.质量:②>③>①>④ |
| D.密度:②>③>④>① |
取五个相同的气球,同温同压下,分别充入CO和以下四种混合气体,吹出体积相等的状况,如图所示。A、B、C、D四个气球内,与CO所含原子数一定相等的是
向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化情况如图所示.则下列说法中不正确的是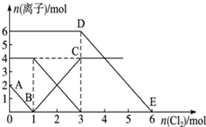
| A.还原性:I->Fe2+>Br- |
| B.原混合溶液中FeBr2的物质的量为3mol |
| C.线段AB表示Fe2+被氯气氧化 |
| D.原溶液中:n(Fe2+):n(I-):n(Br-)═2:1:3 |
某铁的氧化物,用7mol·L-1的盐酸100mL在一定条件下恰好完全溶解,所得溶液再通入0.56 L标准状况下的氯气时,刚好使溶液中Fe2+完全转化为Fe3+,则该氧化物的化学式可表示为
| A.Fe5O7 | B.Fe4O5 | C.Fe2O4 | D.FeO |
在反应:11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,15molCuSO4可氧化磷原子的物质的量为
| A.0.2mol | B.2mol | C.3 mol | D.6mol |
下列描述或表达式正确的是
| A.反应MnO2+ZnS+2H2SO4=MnSO4+ZnSO4+S+2H2O中1molMnO2被氧化转移2mol电子 |
| B.NaHSO4在熔融状态下的电离方程式为:NaHSO4=Na++HSO4- |
| C.不溶于水的盐(CaCO3、BaSO4等)都是弱电解质 |
| D.需要通电才可进行的有:电解、电泳、电离、电镀、电化腐蚀 |