在溶液中,反应A+2B C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)="0.100" mol·L-1,c(B)="0.200" mol·L-1, c(C)="0" mol·L-1。反应物A的浓度随时间的变化如图所示。下列说法正确的是
C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)="0.100" mol·L-1,c(B)="0.200" mol·L-1, c(C)="0" mol·L-1。反应物A的浓度随时间的变化如图所示。下列说法正确的是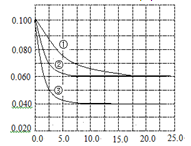
A.若反应①、②的平衡常数分别为K1、K2,则K1< K2
B.反应A+2B C的△H>0
C的△H>0
C.实验②平衡时B的转化率为60%
D.减小反应③的压强,可以使平衡时c(A)="0.060" mol·L-1
下列各组元素性质递变错误的是
| A.Li、Be、B原子最外层电子数逐渐增多 | B.N、O、F氢化物的稳定性依次减弱 |
| C.P、S、Cl最高正价依次升高 | D.Li、Na、K的金属性依次增强 |
NA表示阿伏加德罗常数,下列判断正确的是
| A.在18g18O2中含有NA个氧原子 |
| B.标准状况下,22.4L空气中含有NA个单质分子 |
| C.1molCl2参加反应转移的电子数一定为2NA |
| D.含NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为1mol·L-1 |
某无色气体可能含有H2S、SO2、CO2、HI、HCl气体中的一种或几种。将气体通入氯水后,得无色溶液,向该溶液中滴加氯化钡溶液,有白色沉淀产生。则下列叙述正确的是
| A.该气体中肯定含有H2S和SO2 | B.该气体中肯定含有SO2 |
| C.该气体中肯定含有CO2和SO2 | D.该气体中肯定含有H2S、CO2和HI |
能正确表示下列反应的离子方程式的是
| A.将磁性氧化铁溶于盐酸:Fe3O4+8H+=3Fe3++4H2O |
| B.将氯化亚铁溶液和稀硝酸混合:Fe2++4H++NO3-=Fe3++2H2O+NO↑ |
| C.将铁粉加入稀硫酸中:2Fe+6H+=2Fe3++3H2↑ |
| D.将铜屑加入Fe3+溶液中:2Fe3++Cu=2Fe2++Cu2+ |
下列能在溶液中大量共存的一组离子是
| A.K+、Na+、NO3-、ClO- | B.Fe3+、H+、I-、HCO3- |
| C.NH4+、Ag+、OH-、Cl- | D.Fe2+、Mg2+、SO42-、MnO4- |