如图所示的原电池中,负极发生的反应是
A. + 2e- ="=" Cu + 2e- ="=" Cu |
B.Cu - 2e- ="="  |
C.2 + 2e- ="=" H2↑ + 2e- ="=" H2↑ |
D.Zn - 2e- ="="  |
核黄素又称为维生素B2,可促进发育和细胞再生,有利于增进视力,减轻眼睛疲劳。核黄素分子的结构为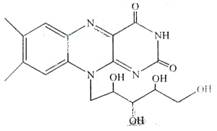
已知: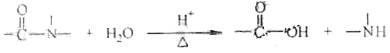
有关核黄素的下列说法中,不正确的是
| A.该化合物的分子式为C17H22N4O6 |
| B.酸性条件下加热水解,有CO2生成 |
| C.酸性条件下加热水解,所得溶液加碱后有NH3生成 |
| D.能发生酯化反应 |
已知I-、Fe2+、SO2、Cl-和H2O2均有还原性,它们在酸性溶液中还原性的强弱顺序为Cl-<Fe2+<H2O2<I-<SO2,则下列反应不能发生的是
| A.2Fe3++SO2+2H2O=2Fe2++SO42-+4H+ |
| B.I2+SO2+2H2O=H2SO4+2HI |
| C.H2O2+H2SO4=SO2+O2+2H2O |
| D.2Fe2++Cl2=2Fe3++2 Cl - |
今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100 mL溶液进行如下实验
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液加热后,收集到气体0.04 mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27 g,经足量盐酸洗涤、干燥后,沉淀质量为2.33 g。根据上述实验,以下推测正确的是
| A.K+可能存在 | B.100 mL溶液中含0.01 mol CO32- |
| C.Cl-可能存在 | D.Ba2+一定不存在,Mg2+可能存在 |
已知在酸性溶液中,下列物质氧化KI时,自身发生如下变化
Fe3+→ Fe2+ MnO4— → Mn2+ Cl2 → Cl— HNO2 → NO
如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是
| A.Fe3+ | B.MnO4— | C.Cl2 | D.HNO2 |
标准状况下VL氨气溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为ρg/mL,质量分数为ω,物质的量浓度为cmol/L,则下列关系中不正确的是
| A.ρ =" (17V" + 22400) / (22.4 + 22.4V) | B.ω =" 17c" / (1000ρ) |
| C.ω =" 17V" / (17V + 22400) | D.c =" 1000Vρ" / (17V + 22400) |