在某些食品包装盒内常有一小包灰黑色粉末。将该粉末溶于盐酸,取上层清液,滴加几滴氯水后,再滴加KSCN溶液,出现血红色。关于该粉末的叙述正确的是
| A.一定含有Fe元素 |
| B.一定含有Mg元素 |
| C.一定禽含有Cu元素 |
| D.一定含有Al元素 |
下列有关金属的说法中不正确的是( )
| A.青铜、不锈钢、硬铝都是合金 |
| B.铜表面易形成致密的氧化膜 |
| C.工业上用电解熔融MgCl2的方法制取金属镁 |
| D.铝是活泼金属,但在空气中耐腐蚀 |
金属冶炼技术随人类对自然界认识的不断深入而发展。下列金属中常用作还原剂冶炼其他金属的是( )
| A.Hg | B.Ag | C.Cu | D.Al |
当光束通过下列分散系时,能产生丁达尔效应的是( )
| A.蔗糖水 | B.食盐水 | C.豆浆 | D.小苏打水 |
下列根据实验操作和现象所得出的结论正确的是
| 选项 |
实验操作 |
实验现象 |
结 论 |
| A |
Al箔插入稀HNO3中 |
无现象 |
Al箔表面被HNO3氧化,形成致密的氧化膜 |
| B |
将某气体通入溴水中 |
溴水颜色褪去 |
该气体一定是乙烯 |
| C |
向饱和Na2CO3中通入足量CO2 |
溶液变浑浊 |
析出了NaHCO3 |
| D |
向装有Fe(NO3)2溶液的试管中加入稀H2SO4 |
在管口观察到红棕色气体 |
HNO3分解成了NO2 |
已知锌及其化合物的性质与铝及其化合物相似。下图横坐标为溶液的pH值,纵坐标为Zn2+或Zn(OH)42-的物质的量浓度的对数。下列说法中不正确的是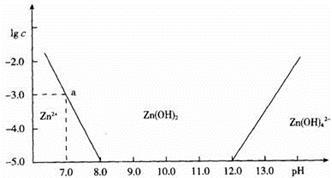
| A.在该温度下,Zn(OH)2的溶度积(Ksp)为1×10―17 |
| B.往1.0L 1.0mol/LZnCl2溶液中加入NaOH固体至pH=6,需NaOH 2.0 mol |
| C.往ZnCl2溶液中加入足量的氢氧化钠溶液,反应的离子方程式为:Zn2++ 4OH―=[Zn(OH)4]2- |
| D.某废液中含Zn2+离子,为提取Zn2+离子可以控制溶液中pH值的范围为8.0~12.0 |