在400℃、101kPa时,NO2(g)+CO(g)=NO(g)+CO2(g)反应过程的能量变化如下图所示。下列说法不正确的是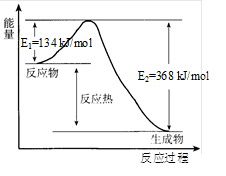
| A.该反应是放热反应 |
| B.该反应的反应热△H=-234 kJ/mol |
| C.加入催化剂,使该反应的活化能降低,反应速率加快,同时使该反应的反应热数值减小 |
D.由图可推出:NO(g)+CO2(g) NO2(g)+CO(g)△H=+234 kJ/mol NO2(g)+CO(g)△H=+234 kJ/mol |
除去NaCl中含有的Ca2 +、Mg2+、SO42-、HCO3-等离子,通常采用以下四种试剂:①Na2CO3 ②BaCl2 ③NaOH ④HCl,加入试剂合理的操作顺序是
+、Mg2+、SO42-、HCO3-等离子,通常采用以下四种试剂:①Na2CO3 ②BaCl2 ③NaOH ④HCl,加入试剂合理的操作顺序是
| A.①②③④ | B.③①②④ |
| C.④②①③ | D.③②①④ |
下图是同学们经常使用的某品牌修正液包装标签。小明仔细阅读后,
结合自己的生活经验和所学知识得出了修正液的某些性质,小明 的
的
推测中不合理的是
| A.修正液的成分对纸张不具腐蚀性 |
| B.修正液中含有有毒的化学物质 |
| C.修正液是一种胶体,均一、稳定 |
| D.修正液的溶剂易挥发、易燃 |
现有三组①CCl4和氯化钠溶液②硝酸钾溶液中含少量氯化钠③氯化钠溶液和碘的水溶液,分离以上各混合液的正确方法依次是
| A.分液、过滤、蒸馏 | B.过滤、结晶、分液 |
| C.蒸馏、分液、萃取 | D.分液、结晶、萃取 |
硅被誉为无机非金属材料的主角,下列物品用到硅单质的是
| A.陶瓷餐具 | B.石英钟表 | C.计算机芯片 | D.光导纤维 |
仅能表示唯一化学反应的离子方程式是
| A.Zn+2H + = Zn2++H2↑ |
| B.CH3COOH+OH-= CH3COO-+H2O |
C.Ba2 ++ 2OH-+ 2H++ SO42-= BaSO4↓+2H2O ++ 2OH-+ 2H++ SO42-= BaSO4↓+2H2O |
| D.CH3COOH + NH3·H2O = CH3COO-+ NH4+ + H2O |