维生素C又叫抗坏血酸,是一种水溶性维生素。在所有维生素中,维生素C是最不稳定的。在贮藏、加工和烹调时.容易被破坏,它还易被氧化和分解。
(1)维生素C的分子式是 ; (2)分子中除酯基外,另一含氧官能团的名称是 。
已知G是合成某高分子化合物的原料,只含C、H、O三种元素,5.9g物质G能与1mol/LNaOH的溶液100mL恰好完全反应,0.1mol物质G与足量金属钠反应在标准状况下生成2.24L氢气,分子结构中含有一个甲基,A的分子式为C8H13O2Br,有机物A、B、C、D、E、F、G之间的相互转化关系如图所示:
⑴写出C的结构简式:.
⑵A中官能团名称是:.
⑶B的同分异构体中属于酯的有多种,任写其中三种属于酯类的结构简式:
,,.
⑷写出D→E化学反应方程式:.
⑸写出反应①化学反应方程式:
⑹写出由F和G 在一定条件下合成高分子化合物的化学反应方程式:
.
注射用双黄连以绿原酸为主要成分(其结构简式如图2)之一,绿原酸有着广泛的药理作用。已知一分子绿原酸在酸性条件下水解得到一分子咖啡酸A(环上有三个取代基,且不完全相邻)和一分子奎尼酸。某小组研究如下:
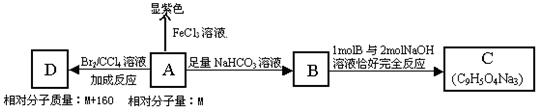
(1)奎尼酸的分子式为_____________。
(2)在图2中方框内补充完整绿原酸的结构
(3)写出咖啡酸与NaHCO3溶液反应的方程式_________ ____。
(4)写出符合下列4个条件的A的同分异构体E的结构简式_____ ________。
③FeCl3溶液反应显紫色②1molE分别能消耗2molNa、1molNaOH
③1molE与足量的新制Cu(OH)2反应可得到2molCu2O
④苯环上的一氯代物只有一种
(5)将一定量咖啡酸A与苯甲酸乙酯的混合物点燃。该混合物完全燃烧消耗x L O2,并生成y g H2O和一定量CO2(气体体积均为标准状况下的体积)。列出混合物中咖啡酸A 的物质的量计算式______________.
杜鹃素主要用于慢性支气管炎及其他痰多咳嗽病症,其结构简式如图所示,其中x、Y表示某种官能团或基团。请回答下列问题:
(1)杜鹃素的分子式可表示为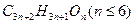 ,则杜鹃素的分为。
,则杜鹃素的分为。
(2)杜鹃素与足量氢氧化钠溶液完全反应,只生成一种有机化合物z和水,化合物Z的摩尔质量为366 g·mol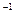 ,则杜鹃素分子中一Y的名称为。
,则杜鹃素分子中一Y的名称为。
(3)有机物A~H满足下列转化关系,芳香烃G的相对分子质量小于110,A与杜鹃素互为同分异构体。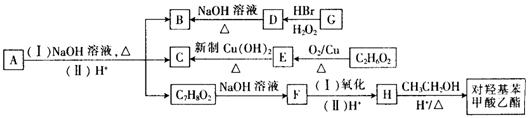
已知:CH3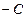 H
H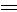 CH2+HBr
CH2+HBr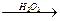 CH3CH2CH2Br
CH3CH2CH2Br
①G的名称为。
②反应D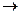 B的化学方程式为
B的化学方程式为 。
。
③A长期露置于空气中容易变质,从分子结构上看,A具有抗氧化作用,则A的结构简
式为。
④符合下列条件的对羟基苯甲酸乙酯的同分异 构体有种(对羟基苯甲酸乙酯自身除外)。
构体有种(对羟基苯甲酸乙酯自身除外)。
Ⅰ.苯环上含有两个对位取代基Ⅱ.能发生水解反应且能与FeCl3溶液发生显色反应
多羟基连在同一个碳原子上易自动失水生成醛或酮
(1)根据上述原理,请写出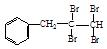 与NaOH的水溶液共热的化学方程式为:;
与NaOH的水溶液共热的化学方程式为:;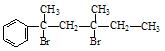 与NaOH的醇溶液共热可以生成种稳定的二烯烃。
与NaOH的醇溶液共热可以生成种稳定的二烯烃。
(2)醛酮在水中可生成水合物: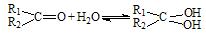 ;这是一个可逆反应,平衡状态(平衡的位置)决定于醛酮的结构。若
;这是一个可逆反应,平衡状态(平衡的位置)决定于醛酮的结构。若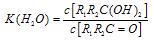 为醛酮的水合平衡常数,其值越大则对应的醛酮水合物越稳定。下表是部分醛、酮的水合平衡常数:
为醛酮的水合平衡常数,其值越大则对应的醛酮水合物越稳定。下表是部分醛、酮的水合平衡常数:
| 化合物 |
  |
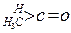 |
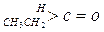 |
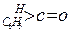 |
| K(H2O) |
2×103 |
1.3 |
0.71 |
8.3×10-3 |
| 化合物 |
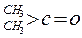 |
 |
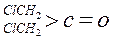 |
 |
| K(H2O) |
2×10-3 |
2.9 |
10 |
很大 |
根据以上表中数据分析,请总结出两条结论:
①。
②。
(3)工业上生产苯甲醛 有以下两种方法:
有以下两种方法:
与方法①相比,方法②的优点是,
缺点是。
(4)苯腙是有机染料的主要原料,由醛(或酮)与苯肼生成苯腙的反应为:
反应①的原子利用率为100%,则中间产物A的结构简式为;
反应②的反应类型属于。
(5)由对苯二甲醛的氧化产物“对苯二甲酸”与“乙二醇”缩聚,生成的聚酯纤维(涤纶)
的结构简式为。
异丙苯(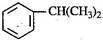 ),是一种重要的有机化工原料。
),是一种重要的有机化工原料。
根据题意完成下列填空:
(1)由苯与2-丙醇反应制备异丙苯属于反应;由异丙苯制备对溴异丙苯的反应试剂和反应条件为。
(2)异丙苯有多种同分异构体,其中一溴代物最少的芳香烃的名称是。
(3)α-甲基苯乙烯(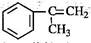 )是生产耐热型ABS树脂的一种单体,工业上由异丙苯催化脱氢得到。写出由异丙苯制取该单体的另一种方法(用化学反应方程式表示)。
)是生产耐热型ABS树脂的一种单体,工业上由异丙苯催化脱氢得到。写出由异丙苯制取该单体的另一种方法(用化学反应方程式表示)。
(4)耐热型ABS树脂由丙烯腈(CH2=CHCN)、1,3-丁二烯和α-甲基苯乙烯共聚生成,写出该树脂的结构简式(不考虑单体比例)。