氢元素与其他元素形成的二元化合物称为氢化物,下面关于氢化物的叙述正确的是( )
| A.一个D2O分子所含有的中子数为8 | B.热稳定性:H2S >HF |
C.NH3的结构式为: |
D.HCl的电子式为: 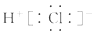 |
丰富多彩的颜色变化增添了化学实验的魅力,下列有关反应颜色变化的叙述中,正确的是
①新制氯水久置后→浅黄绿色消失
②淀粉溶液遇碘化钾→蓝色
③蔗糖中加入浓硫酸搅拌→白色
④SO2通入品红溶液中→红色褪去
⑤氨气通入酚酞溶液中→红色
| A.①②④⑤ | B.②③④⑤ | C.①④⑤ | D.①②③④⑤ |
相同条件下,质量相同的NH3和CH4,下列说法正确的是
| A.密度比为16:17 | B.氢原子比为3:4 |
| C.物质的量比为1:1 | D.体积比为16:17 |
只用一种试剂即可区别Na2SO4、MgCl2、FeCl2、Al2(SO4)3、(NH4)2SO4五种溶液,这种试剂是
| A.BaCl2 | B.H2SO4 | C.NaOH | D.AgNO3 |
下列溶液中能用来区别SO2和CO2气体的是
①澄清的石灰水②氢硫酸③氯水④酸性高锰酸钾溶液⑤氯化钡溶液⑥品红溶液
| A.①⑤ | B.③④⑤ | C.②⑥ | D.②③④⑥ |
一种盐X与氢氧化钠溶液共热,可放出气体Y,Y经过一系列氧化后再溶于水可得Z溶液,Y和Z溶液反应又生成X,则X可能是
| A.NH4NO3 | B.NH4Cl | C.NH4HCO3 | D.(NH4)2CO3 |