下列有关实验操作、现象和解释或结论都正确的是
| 选项 |
实验操作 |
现象 |
解释或结论 |
| A |
过量的Fe粉中加入稀HNO3,充分反应后,滴入KSCN溶液 |
溶液呈红色 |
稀HNO3将Fe氧化为Fe3+ |
| B |
5mL4%的过氧化氢溶液中加入少量MnO2粉末 |
迅速产生大量气泡 |
催化剂能显著地增大化学反应速率 |
| C |
Al箔插入稀HNO3中 |
无现象 |
Al箔表面被HNO3氧化,形成致密的氧化膜 |
| D |
用石墨棒做电极,电解氯化铜溶液 |
产生使湿润的淀粉碘化钾试纸变蓝的黄绿色气体 |
该气体为Cl2,放出该气体的电极为电解池的阳极 |
有关如图所示原电池(盐桥中装有含琼脂的KCl饱和溶液)的叙述,正确的是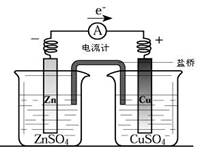
| A.铜是阳极,铜片上有气泡产生 |
| B.铜离子在铜片表面被还原 |
| C.电流从锌片经导线流向铜片 |
| D.反应中,盐桥中的K+会移向ZnSO4溶液 |
钢铁发生吸氧腐蚀时,正极上发生的电极反应是
| A.2H++2e— ===H2 ↑ | B.Fe-2e—===Fe2+ |
| C.2H2O+O2+4e— ===4OH— | D.Fe-3e—===Fe3+ |
为了探究影响化学反应速率的因素,4位同学分别设计了下列4个实验,其中结论不正确的是
| A.将大小、形状相同的镁条和铝条与相同浓度、相同温度下的盐酸反应时,两者快慢相同 |
| B.盛有相同浓度双氧水的两支试管,一支加入MnO2放在冷水中,一支直接放在冷水中,前者反应快 |
| C.将浓硝酸分别放在冷暗处和强光下,发现强光下的浓硝酸分解得快 |
| D.升高温度,H2O2的分解速率加快,原因是反应物分子的能量增加,活化分子百分数增大,有效碰撞次数增多 |
下列与化学反应能量变化相关的叙述正确的是
| A.生成物能量一定低于反应物总能量 |
| B.放热反应不必加热就一定能发生 |
| C.应用盖斯定律,可计算某些难以直接测量的反应的焓变 |
| D.同温同压下,H2(g)+Cl2(g)===2HCl(g)在光照和点燃条件的ΔH不同 |
下列叙述正确的是
| A.推广使用太阳能、风能、海洋能、氢能,有利于缓解温室效应 |
| B.乙醇和汽油都是可再生能源,应大力推广“乙醇汽油” |
| C.废电池需回收,主要是要利用电池外壳的金属材料 |
| D.升高温度可降低活化能 |