反应A(g)+B(g) C(g) +D(g) 发生过程中的能量变化如图,△H表示反应的焓变。下列说法正确的是( )
C(g) +D(g) 发生过程中的能量变化如图,△H表示反应的焓变。下列说法正确的是( )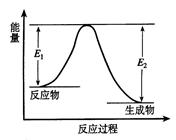
| A.反应体系中加入催化剂,反应速率增大,E1减小,E2增大 |
| B.反应体系中加入催化剂,反应速率增大,△H不变 |
| C.△H < 0,反应达到平衡时,升高温度,A的转化率增大 |
| D.反应达到平衡时,加入A,再次平衡时A的转化率增大 |
X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示。若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是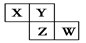
| A.原子半径:W>Z>Y>X |
| B.最高价氧化物对应水化物的酸性W比Z弱 |
| C.Y的气态氢化物的稳定性较Z的弱 |
| D.四种元素的单质中,Z的熔点最高 |
根据下表信息,判断以下叙述正确的是
部分短周期元素的原子半径及主要化合价
| 元素代号 |
L |
M |
Q |
R |
T |
| 原子半径/nm |
0.160 |
0.143 |
0.112 |
0.104 |
0.066 |
| 主要化合价 |
+2 |
+3 |
+2 |
+6、-2 |
-2 |
A.氢化物的沸点为H2T<H2R B.单质与稀盐酸反应的速度为L<Q
C.M与T形成的化合物具有两性D.L2+与R2-的核外电子数相等
在标准状况下将1.92g铜粉投入一定量浓HNO3中随着铜粉的溶解,反应生成的气体颜色逐渐变浅,当铜粉完全溶解后共收集到由NO2和NO组成的混和气体1.12L,则混和气体中NO的体积为
| A.112mL | B.1008mL | C.224mL | D.448mL |
下列物质之间的转化符合:“甲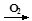 乙
乙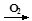 丙
丙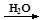 丁”的组合是
丁”的组合是
①Na→NaOH; ②Cu→Cu(OH)2;③S→H2SO4;④NH3→HNO3
| A.①②③ | B.①③④ | C.②③④ | D.全部 |
如右图所示,夹子开始处于关闭状态,将液体A滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了,则液体A和气体B的组合不可能是下列的
| A.氢氧化钠溶液、二氧化碳 | B.水、氨气 |
| C.氢氧化钠溶液、一氧化氮 | D.水、二氧化氮 |