下图是锌片和铜片在稀硫酸中所组成的原电池装置,c、d为两个电极。下列有关的判断不正确的是( )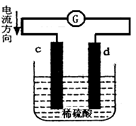
| A.电池工作的过程中,d电极上产生气泡 |
| B.电池工作时,溶液中SO42-向d移动 |
| C.c为负极,发生氧化反应 |
| D.电池工作的过程中,溶液中SO42-浓度基本不变 |
下列有关晶体的叙述错误的是( )
| A.离子晶体中,一定存在离子键 |
| B.原子晶体中,只存在共价键 |
| C.金属晶体的熔沸点均很高 |
| D.稀有气体的原子能形成分子晶体 |
下列性质中,可以证明某化合物内一定存在离子键的是( )
| A.可溶于水 |
| B.具有较高的熔点 |
| C.水溶液能导电 |
| D.熔融状态能导电 |
与Ne的核外电子排布相同的离子跟与Ar的核外电子排布相同的离子所形成的化合物是( )
| A.MgBr2 | B.Na2S | C.KCl | D.KF |
下列各式是用电子式表示的对应物质形成的过程,其中正确的是( )
A.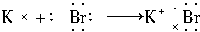 |
B. 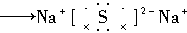 |
C.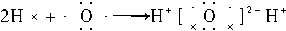 |
D.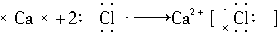 |
下列说法中正确的是( )
| A.完全由非金属元素组成的化合物不一定是共价化合物 |
| B.构成分子晶体的粒子一定含有共价键 |
| C.分子晶体的熔点一定比金属晶体的熔点低 |
| D.含有金属离子的晶体一定是离子晶体 |