下列叙述中错误的是:
| A.原子半径 Na>Si>Cl | B.稳定性 SiH4<HCl<H2S |
| C.金属性 Na>Mg>Al | D.酸性 H3PO4<H2SO4<HClO4 |
下列各组中的反应,属于同一反应类型的是
| A.乙烷和氯气制氯乙烷;乙烯与氯化氢反应制氯乙烷 |
| B.乙醇和乙酸制乙酸乙酯;苯的硝化反应 |
| C.葡萄糖与新制氢氧化铜共热;蔗糖与稀硫酸共热 |
| D.乙醇和氧气制乙醛;苯和氢气制环己烷 |
分子式为C3H4Cl2链状有机物的同分异构体共有(不考虑顺反异构)
| A.4种 | B.5种 | C.6种 | D.7种 |
下列对有关实验的描述不正确的是
| A.在浓氨水中加入生石灰可以制取少量的NH3 |
| B.用水就可以一次性鉴别溴苯、苯、乙酸三种物质 |
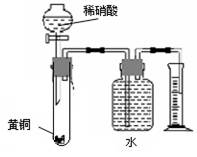
| C.用如下图所示的装置可以测定黄铜(Cu、Zn合金)中Zn的含量 |
| D.除去粗盐中的Ca2+、Mg2+、SO42-,依次加入的物质可以是H2O、 Ba(OH)2、Na2CO3、HCl |
下列各组物质的分类正确的是
| A.同位素:1H+、2H2、3H |
| B.同系物:丙烷、异丁烷、新戊烷 |
| C.电解质:冰醋酸、水银、烧碱 |
| D.酸性氧化物:一氧化氮﹑二氧化碳、三氧化硫 |
如图为某有机物的结构简式。已知酯类在铜铬氧化物(CuO·CuCrO4)催化下,与氢气反应得到醇,羰基双键可同时被还原,但苯环在催化氢化过程中不变,其反应原理如下:在铜铬氧化物催化下,R1COOR2 + 2H2→R1CH2OH + R2OH
关于该化合物的下列说法中,正确的是()
A.该有机物的化学式为C20H 14O5,该有机物可以属于酯类、酚类、醚类 14O5,该有机物可以属于酯类、酚类、醚类 |
| B.该有机物可以与浓溴水发生加成反应 |
C.1mol该有机物在铜铬氧化物催化下仅能与2mol氢 气发生反应 气发生反应 |
| D.与足量氢氧化钠溶液充分反应,1mol该有机物最多可以与5molNaOH反应,所得产物中有醇类物质 |