甲乙两同学学完质量守恒定律后设计了如下实验探究质量守恒定律。
(1)甲同学取一支蜡烛粘在一小块玻璃片上,将玻璃片和蜡烛一起放在天平上称量。天平平衡,如图所示。点燃蜡烛,过一会观察到天平指针_______(向左偏、向右偏)因此他得出结论:蜡烛燃烧不符合质量守恒定律。
(2)乙同学对甲同学的实验思考后,进行了改进,他将蜡烛放于一密闭、干燥、透明的玻璃容器中,放于天平上调节平衡,并设法点燃蜡烛,过一会观察到蜡烛熄灭,天平仍然平衡,他得出结论,蜡烛燃烧符合质量守恒定律。
(3)甲同学得出不符合质量守恒定律的原因是 ______________。乙同学从实验上证实蜡烛燃烧符合质量守恒定律。并且还从微观角度进行了解释,他的解释是____________________。
(4)乙同学通过仔细观察。还观察到了一个明显的现象_______________,他根据该现象得出蜡烛的组成中含有氢元素;该同学又进行了进一步的实验,最后还得出蜡烛的组成中还一定含碳元素。他进行的实验是_________________。他得出蜡烛的组成中一定含碳、氢元素结论的化学原理是_______________________。
(5)乙同学实验时,观察到蜡烛熄灭,蜡烛熄灭的原因是______________。请你举出生活中应用该原理灭火的一个具体事例____________________。
(6分)某同学对含有泥沙和碳酸钠的粗盐进行提纯并配制一定质量分数的NaCl溶液,
请回答:
(1)除去粗盐中混有的泥沙的主要操作的顺序依次为下图中的(填字母)__________。
(2)写出上图中标注的仪器的名称a____________________,b____________________。
(3)在上图C操作中玻璃棒搅拌的作用是________________________________________。
(4)若得到产品的产率偏低( ),下列原因不可能的是_____。
),下列原因不可能的是_____。
| A.过滤时滤纸有破损 |
| B.蒸发时过早停止加热,产品中仍残留水分 |
| C.溶解粗盐时,加入的水量不足 |
| D.未将所有产品都转移出蒸发皿进行称量 |
(5)为了除去粗盐中的碳酸钠,应该在过滤前向烧杯中加适量的__________溶液(填化学式)。
(6)用所得氯化钠晶体配制一定溶质质量分数的氯化钠溶液,需要的玻璃仪器有烧杯、玻璃棒、滴管和__________。
(1)请你与小明和他的同学一起进行实验室制取二氧化碳的探究.
小明对三组药品进行了研究,实验记录如下:
| 组别 |
药品 |
实验现象 |
| ① |
块状石灰石和稀盐酸 |
产生气泡速率适中 |
| ② |
块状石灰石和稀硫酸 |
产生气泡速率缓慢并逐渐停止 |
| ③ |
碳酸钠粉末和稀盐酸 |
产生气泡速率很快 |
从制取和收集的角度分析,一般选择第①组药品,所发生反应的化学方程式为;不选择第③组药品的原因是.
(2)老师为他们提供的如图1所示的实验仪器(导管、橡皮塞等未画出).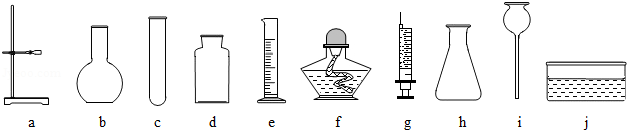
小明根据提供的实验仪器分别设计了如图2所示四套制取和收集二氧化碳的装置.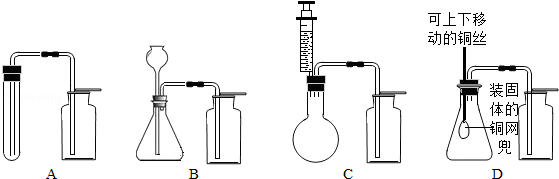
对上面的设计方案小明和他的同学进行了交流讨论.
其中可能收集不到二氧化碳气体的装置是;能够使反应随时停止和发生的装置是.用澄清石灰水可鉴定CO2气体,请写出其化学方程式为.
反思小结:
气体制取和收集装置的选择依据 .
.
某化学兴趣小组进行研究性学习,探究热水壶中的水垢。
【查阅资料】①天然水中一般都含有Ca2+、Mg2+、HCO3-等离子,在加热时,这些离子反应生成溶解度更小的物质—水垢[Mg(OH)2和CaCO3]。②碱石灰是氧化钙和氢氧化钠的固体混合物。
【实验设计】
1、按图组装仪器,将10.8g水垢样品放入装置B中,在装置D中加入一定量的稀盐酸溶液;
2、将稀盐酸溶液缓缓滴入装置B中,与水垢充分反应;
3、待实验不再产生气泡时,打开AB间活塞,从左端缓缓鼓入一定量的空气;
4、吹扫一段时间后,测定到装置E质量增重了2.2g。
【分析数据】
(1)仪器a的名称是___________;
(2)鼓入空气的目的是__________;装置A的作用是_______;装置C中体现浓硫酸的__________性;
(3)写出实验中产生气体的化学反应方程式:_______________________;
(4)水垢中Mg(OH)2的质量为__________。
化学兴趣小组的同学对实验室一瓶没有标签的银白色金属X,展开探究活动。
【实验目的】X金属活动性顺序中的相对位置关系。
【实验探究】取形状、大小相同的X、Cu 、Zn三种金属薄片,用砂纸打磨光亮,分别放入三份等体积、等质量分数的稀硫酸溶液中,观察现象。
| 实验 |
X放入稀硫酸中 |
Zn放入稀硫酸中 |
Cu放入稀硫酸中 |
| 实验现象 |
金属X表面产生气泡缓慢 |
金属锌表面产生气泡较快 |
金属铜表面无气泡 |
【实验结论】三种金属在金属活动性顺序中的相对位置由弱到强的是。
【问题与思考】用砂纸打磨金属片的目的是。
【拓展探究】
(1)兴趣小组的同学将锌片放入一定量和混合溶液中,反应一段时间后,过滤,对蓝色滤液的组成进行探究。
(2)猜想:①滤液中的溶质为硝酸锌和硝酸铜;
②滤液中的溶质为硝酸锌、硝酸铜和硝酸银。
(3)请你完成下面实验,验证猜想②成立。
| 实验操作 |
实验现象 |
实验结论 |
| 取少量的滤液于试管中,在滤液中加入。 |
猜想②成立 |
【归纳总结】锌和硝酸银溶液反应的化学方程式是。
小林同学在做探究质量守恒定律实验时,称取2.4g镁条在点燃的条件下与充足的空气反应,其反应的化学方程式为______________________________.实验完毕后,称得所得固体的质量小于4.0g.
【提出问题】固体质量为什么会小于4.0g呢?是否发生了其他反应呢?
【查阅资料】镁在空气中燃烧时,除了镁与氧气反应外,还可发生反应:
①2Mg+CO2点燃C+2MgO ② 3Mg+N2点燃Mg3N2
【猜想与假设】反应后固体质量小于4.0g是由于发生反应_______(填“①”或“②”)造成的,其理由是_____________________________.
【实验探究】根据初中化学所学知识用图所示装置除去空气中的氧气得到氮气(含少量稀有气体).可燃物应选择的物质是_________(填写物质的字母代号).
A.木炭B.红磷C.硫粉
选择的理由是________________________________________;
将点燃的镁条伸入所制得的氮气中,镁条在氮气中剧烈燃烧.
【实验结论】2.4g镁在空气中完全反应后所得固体质量小于4.0g,是由于生成的产物是___________的混合物所致.