W、X、Y、Z是原子序数依次增大的短周期元素,X、Y是金属元素,X的焰色呈黄色。W、Z最外层电子数相同,Z的核电荷数是W的2倍。Y原子核外无未成对电子,则下列说法不正确的是 ( )
| A.X熔点比Y低 |
| B.Z和W可形成原子个数比为1∶2和1∶3的共价化合物,且两种化合物中Z原子的杂化类型相同。 |
| C.Y能与干冰反应,且只生成白色的固体 |
| D.X、Y和Z三种元素形成的最高价氧化物对应的水化物能两两反应 |
下表中,对陈述I、II的正确性及两者间有无因果关系的判断都正确的是
| 选项 |
陈述I |
陈述II |
判断 |
| A |
用锌和足量稀硫酸制取氢气时加入硫酸铜溶液 |
可以制取更多的氢气 |
I对、II对、有 |
| B |
用Mg—Al—NaOH构成原电池 |
Mg更活泼作负极 |
I对、II对、无 |
| C |
AlCl3是离子化合物 |
电解熔融的AlCl3制取金属铝 |
I对、II对、无 |
| D |
石墨常用做电解池的电极 |
石墨的化学性质稳定且导电性好 |
I对、II对、有 |
下图各容器中盛有海水,铁在其中被腐蚀时由快到慢的顺序是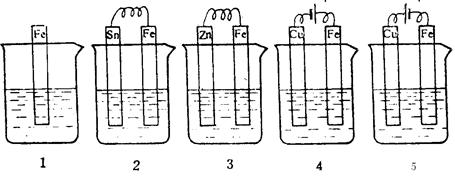
| A.4>2>1>3>5 | B.2>1>5>3>4 |
| C.5>4>2>3>1 | D.3>5>2>4>1 |
常温下,柠檬水溶液的PH是3,其中水电离的c(H+)为
| A.1×10-3mol/L | B.1×10-7mol/L |
| C.1×10-11mol/L | D.1×10-14mol/L |
在一密闭容器中进行如下反应:2SO2(气)+O2(气) 2SO3(气),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是
2SO3(气),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是
| A.SO2为0.4mol/L、O2为0.2mol/L | B.SO2为0.25mol/L |
| C.SO2、SO3均为0.15mol/L | D.SO3为0.4mol/L |
在容积一定的密闭容器中发生可逆反应A(g)+2B(g) 2C(g);△H>0,平衡移动关系如图所示。下列说法正确的是:
2C(g);△H>0,平衡移动关系如图所示。下列说法正确的是:
| A.P1>P2,纵坐标指A的质量分数 |
| B.P1> P2,纵坐标指C的质量分数 |
| C.P1< P2,纵坐标指A的转化率 |
| D.P1< P2,纵坐标指混合气体的平均摩尔质量 |