研究人员研制出一种锂水电池,可作为鱼雷和潜艇的储备电源。该电池以金属锂和钢板为电极材料,以LiOH为电解质,使用时加入水即可放电。关于该电池的下列说法不正确的是( )
| A.水既是氧化剂又是溶剂 | B.放电时正极上有氢气生成 |
| C.放电时,正极附近碱性减弱 | D.总反应为:2Li+2H2O===2LiOH+H2↑ |
加热聚丙烯废塑料可以得到碳、氢气、甲烷、乙烯、丙烯、苯和甲苯。用图所示装置探究废旧塑料的再利用。
下列叙述不正确的是
| A.聚丙烯的链节是—CH2—CH2—CH2— |
| B.装置乙的试管中可收集到芳香烃 |
| C.装置丙中可得到卤代烃 |
| D.最后收集的气体可做燃料 |
下列关于有机化合物的说法不正确的是
| A.鸡蛋清中加浓硝酸微热后变黄 |
| B.将苯滴入溴水中,振荡后水层接近无色 |
| C.蛋白质水解能得到氨基酸 |
| D.苯与乙烯都能使高锰酸钾溶液褪色 |
2008奥运会吉样物福娃,其外材为纯羊毛线.内充物为无毒的聚酯纤维(结构简式如下图)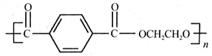
下列说法中正确的是
| A.羊毛与聚酯纤维的化学成分相同 |
| B.聚酯纤维和羊毛在一定条件下均能水解 |
| C.该聚酯纤维的单体为对苯二甲酸和乙醇 |
| D.聚酯纤维和羊毛都属于天然高分子材料 |
一定条件下发生反应A(g)+3B(g) = 2C(g);△H =" a" kJ·mol-1,现有1molA(g)和3molB(g)反应生成2molC(g),反应过程能量变化如图所示,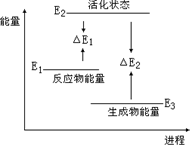
下列说法正确的是
| A.该反应为放热反应,a=E1-E3。 |
| B.该反应为放热反应, a=E2-E1 |
| C.该反应为放热反应, a=△E1-△E2 |
| D.该反应为吸热反应, a=△E2-△E1 |
(8分每空2分)恒温恒容下2 mol A气体和2 mol B气体通入体积为2 L的密闭容器中发生如下反应:2A(g) + B(g) 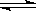 xC(g) + 2D(s)。2 min时反应达到平衡状态,此时剩余1.2 mol B,并测得C的浓度为1.2 mol/L。
xC(g) + 2D(s)。2 min时反应达到平衡状态,此时剩余1.2 mol B,并测得C的浓度为1.2 mol/L。
(1)从开始反应至达到平衡状态,生成C的平均反应速率为。
(2)x=。
(3)A的转化率为。
(4)下列各项可作为该反应达到平衡状态的标志的是(填各项代号,错选不计分)。
| A.压强不再变化 |
| B.A的消耗速率与B的消耗速率之比为2∶1 |
| C.气体密度不再变化 |
| D.B的体积分数不变 |